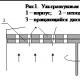
Spezifische volumetrische Wärmekapazität von Luft. Dynamische und kinematische Viskosität von Luft bei verschiedenen Temperaturen. Luftfeuchtigkeit. Wärmekapazität und Enthalpie der Luft
Was notwendig ist, um die Temperatur des Arbeitsmediums, in diesem Fall Luft, um ein Grad zu ändern. Die Wärmekapazität der Luft ist direkt abhängig von Temperatur und Druck. Gleichzeitig können verschiedene Methoden verwendet werden, um verschiedene Arten von Wärmekapazitäten zu untersuchen.
Mathematisch wird die Wärmekapazität von Luft als Verhältnis der Wärmemenge zum Temperaturanstieg ausgedrückt. Die Wärmekapazität eines Körpers mit einer Masse von 1 kg wird als spezifische Wärme bezeichnet. Die molare Wärmekapazität von Luft ist die Wärmekapazität von einem Mol eines Stoffes. Die Wärmekapazität wird angezeigt - J / K. Molare Wärmekapazität bzw. J / (mol * K).
Die Wärmekapazität kann als physikalische Eigenschaft eines Stoffes, in diesem Fall Luft, angesehen werden, wenn die Messung unter konstanten Bedingungen durchgeführt wird. Meistens werden solche Messungen bei konstantem Druck durchgeführt. So wird die isobare Wärmekapazität von Luft bestimmt. Sie steigt mit steigender Temperatur und steigendem Druck und ist auch eine lineare Funktion dieser Größen. In diesem Fall erfolgt die Temperaturänderung bei konstantem Druck. Zur Berechnung der isobaren Wärmekapazität ist es notwendig, die pseudokritische Temperatur und den Druck zu bestimmen. Sie wird anhand von Referenzdaten ermittelt.
Wärmekapazität der Luft. Besonderheiten
Luft ist ein Gasgemisch. Bei ihrer Berücksichtigung in der Thermodynamik wurden die folgenden Annahmen getroffen. Jedes Gas in der Mischung muss gleichmäßig über das Volumen verteilt sein. Somit ist das Volumen des Gases gleich dem Volumen der gesamten Mischung. Jedes Gas in der Mischung hat seinen eigenen Partialdruck, den es auf die Gefäßwände ausübt. Jede der Komponenten des Gasgemisches muss eine Temperatur haben, die gleich der Temperatur des gesamten Gemisches ist. In diesem Fall ist die Summe der Partialdrücke aller Komponenten gleich dem Druck der Mischung. Die Berechnung der Wärmekapazität von Luft erfolgt auf der Grundlage von Daten zur Zusammensetzung des Gasgemisches und der Wärmekapazität einzelner Komponenten.
Die Wärmekapazität charakterisiert einen Stoff mehrdeutig. Aus dem ersten Hauptsatz der Thermodynamik können wir schließen, dass die innere Energie eines Körpers nicht nur von der aufgenommenen Wärmemenge, sondern auch von der vom Körper verrichteten Arbeit abhängt. Unter verschiedenen Bedingungen des Wärmeübertragungsprozesses kann die Arbeit des Körpers variieren. Somit kann die gleiche Wärmemenge, die dem Körper zugeführt wird, Änderungen der Temperatur und der inneren Energie des Körpers verursachen, die sich im Wert unterscheiden. Dieses Merkmal ist nur für gasförmige Stoffe charakteristisch. Im Gegensatz zu Feststoffen und Flüssigkeiten können gasförmige Substanzen das Volumen stark ändern und Arbeit verrichten. Deshalb bestimmt die Wärmekapazität der Luft die Art des thermodynamischen Prozesses selbst.
Bei konstantem Volumen verrichtet die Luft jedoch keine Arbeit. Daher ist die Änderung der inneren Energie proportional zur Änderung seiner Temperatur. Das Verhältnis der Wärmekapazität in einem Prozess mit konstantem Druck zur Wärmekapazität in einem Prozess mit konstantem Volumen ist Teil der adiabatischen Prozessformel. Es wird mit dem griechischen Buchstaben Gamma bezeichnet.
Aus der Geschichte
Die Begriffe „Wärmekapazität“ und „Wärmemenge“ beschreiben ihr Wesen nicht sehr gut. Dies liegt daran, dass sie aus der im 18. Jahrhundert populären Kalorientheorie in die moderne Wissenschaft gelangten. Die Anhänger dieser Theorie betrachteten Wärme als eine Art unwägbare Substanz, die in Körpern enthalten ist. Diese Substanz kann weder zerstört noch geschaffen werden. Die Abkühlung und Erwärmung von Körpern wurde durch eine Abnahme bzw. Zunahme des Kaloriengehalts erklärt. Im Laufe der Zeit wurde diese Theorie als unhaltbar erkannt. Sie konnte nicht erklären, warum die gleiche Änderung der inneren Energie eines Körpers bei der Übertragung unterschiedlicher Wärmemengen auf ihn auftritt und auch von der Arbeit des Körpers abhängt.
Labor Nr. 1
Definition von Masse isobar
Luftwärmekapazität
Die Wärmekapazität ist die Wärme, die einer Mengeneinheit eines Stoffes zugeführt werden muss, um sie um 1 K zu erwärmen. Eine Mengeneinheit eines Stoffes kann in Kilogramm, Kubikmeter unter normalen physikalischen Bedingungen und Kilomol gemessen werden. Ein Kilomol eines Gases ist die Masse eines Gases in Kilogramm, numerisch gleich seinem Molekulargewicht. Somit gibt es drei Arten von Wärmekapazitäten: Masse c, J/(kg⋅K); Volumen c', J/(m3⋅K) und molar, J/(kmol⋅K). Da ein Kilomol Gas eine μ-fache Masse von mehr als einem Kilogramm hat, wird auf eine gesonderte Bezeichnung für die molare Wärmekapazität verzichtet. Beziehungen zwischen Wärmekapazitäten:
wobei = 22,4 m3/kmol das Volumen eines Kilomols eines idealen Gases unter normalen physikalischen Bedingungen ist; ist die Dichte des Gases unter normalen physikalischen Bedingungen, kg/m3.
Die wahre Wärmekapazität eines Gases ist die Ableitung der Wärme nach der Temperatur:
Die dem Gas zugeführte Wärme hängt vom thermodynamischen Prozess ab. Sie lässt sich aus dem ersten Hauptsatz der Thermodynamik für isochore und isobare Prozesse bestimmen:
Dabei wird die Wärme 1 kg Gas im isobaren Prozess zugeführt; ist die Änderung der inneren Energie des Gases; ist die Arbeit von Gasen gegen äußere Kräfte.
Formel (4) formuliert im Wesentlichen den 1. Hauptsatz der Thermodynamik, woraus die Mayer-Gleichung folgt:
Wenn wir = 1 K setzen, dann ist die physikalische Bedeutung der Gaskonstante die Arbeit von 1 kg Gas in einem isobaren Prozess, wenn sich seine Temperatur um 1 K ändert.
Mayers Gleichung für 1 Kilomol Gas ist
wobei = 8314 J/(kmol⋅K) die universelle Gaskonstante ist.
Zusätzlich zur Mayer-Gleichung sind die isobaren und isochoren Massenwärmekapazitäten von Gasen durch den Adiabatenindex k (Tabelle 1) miteinander verbunden:
Tabelle 1.1
Werte der adiabatischen Exponenten für ideale Gase
Atomizität von Gasen | |
Einatomige Gase | |
Zweiatomige Gase | |
Drei- und mehratomige Gase |
ZWECK DER ARBEIT
Vertiefung des theoretischen Wissens über die Grundgesetze der Thermodynamik. Praktische Entwicklung der Methode zur Bestimmung der Wärmekapazität von Luft anhand der Energiebilanz.
Experimentelle Bestimmung der spezifischen Massenwärmekapazität von Luft und Vergleich des erhaltenen Ergebnisses mit einem Referenzwert.
1.1. Beschreibung des Laboraufbaus
Die Installation (Abb. 1.1) besteht aus einem Messingrohr 1 mit einem Innendurchmesser d =
= 0,022 m, an deren Ende sich eine elektrische Heizung mit Wärmedämmung befindet 10. Im Inneren des Rohres bewegt sich ein Luftstrom, der zugeführt wird 3. Der Luftstrom kann durch Änderung der Lüftergeschwindigkeit gesteuert werden. Im Rohr 1 ist ein Rohr für vollen Druck 4 und überschüssigen statischen Druck 5 installiert, die mit Manometern 6 und 7 verbunden sind. Außerdem ist im Rohr 1 ein Thermoelement 8 installiert, das sich gleichzeitig mit dem entlang des Querschnitts bewegen kann voller Druckschlauch. Der EMF-Wert des Thermoelements wird durch das Potentiometer 9 bestimmt. Die Erwärmung der durch das Rohr strömenden Luft wird mit einem Laborautotransformator 12 gesteuert, indem die Heizleistung geändert wird, die durch die Messwerte des Amperemeters 14 und des Voltmeters 13 bestimmt wird. Die Lufttemperatur am Ausgang des Erhitzers wird durch das Thermometer 15 bestimmt.
1.2. EXPERIMENTELLE TECHNIK
Wärmestrom der Heizung, W:
wo ich aktuell bin, A; U – Spannung, V; = 0,96; =
= 0,94 - Wärmeverlustkoeffizient.

Abb.1.1. Schema des Versuchsaufbaus:
1 - Rohr; 2 - Verwirrer; 3 – Lüfter; 4 - Rohr zur Messung des dynamischen Kopfes;
5 - Abzweigrohr; 6, 7 – Differenzdruckmanometer; 8 - Thermoelement; 9 - Potentiometer; 10 - Isolierung;
11 - elektrische Heizung; 12 – Laborspartransformator; 13 - Voltmeter;
14 - Amperemeter; 15 - Thermometer
Von Luft empfundener Wärmestrom, W:
wobei m der Luftmassenstrom in kg/s ist; – experimentelle, massenisobare Wärmekapazität von Luft, J/(kg·K); – Lufttemperatur am Ausgang des Heizabschnitts und am Eingang in ihn, °C.
Luftmassenstrom, kg/s:
![]() . (1.10)
. (1.10)
Hier ist die durchschnittliche Luftgeschwindigkeit im Rohr, m/s; d ist der Innendurchmesser des Rohrs, m; - Luftdichte bei Temperatur , die durch die Formel gefunden wird, kg/m3:
![]() , (1.11)
, (1.11)
wobei = 1,293 kg/m3 die Luftdichte unter normalen physikalischen Bedingungen ist; B – Druck, mm. rt. St.; - zu hoher statischer Luftdruck im Rohr, mm. Wasser. Kunst.
Die Luftgeschwindigkeiten werden durch die dynamische Höhe in vier gleichen Abschnitten, m/s, bestimmt:
Wo ist der dynamische Kopf, mm. Wasser. Kunst. (kgf/m2); g = 9,81 m/s2 ist die Freifallbeschleunigung.
Mittlere Luftgeschwindigkeit im Rohrabschnitt, m/s:
Die durchschnittliche isobare Massenwärmekapazität von Luft wird aus Formel (1.9) bestimmt, in die der Wärmestrom aus Gleichung (1.8) eingesetzt wird. Den genauen Wert der Wärmekapazität von Luft bei einer durchschnittlichen Lufttemperatur erhält man nach der Tabelle der durchschnittlichen Wärmekapazitäten oder nach der Summenformel J / (kg⋅K):
![]() . (1.14)
. (1.14)
Relativer Fehler des Experiments, %:
![]() . (1.15)
. (1.15)
1.3. Durchführung des Experiments und Verarbeitung
Messergebnisse
Das Experiment wird in der folgenden Reihenfolge durchgeführt.
1. Das Laborstativ wird eingeschaltet und nachdem der stationäre Modus hergestellt wurde, werden die folgenden Messwerte genommen:
Dynamischer Luftdruck an vier Punkten gleicher Rohrabschnitte;
Zu hoher statischer Luftdruck im Rohr;
Strom I, A und Spannung U, V;
Einlasslufttemperatur, °С (Thermoelement 8);
Austrittstemperatur, °С (Thermometer 15);
Luftdruck B, mm. rt. Kunst.
Das Experiment wird für den nächsten Modus wiederholt. Die Messergebnisse sind in Tabelle 1.2 eingetragen. Berechnungen werden in der Tabelle durchgeführt. 1.3.
Tabelle 1.2
Maßtabelle
Wertname | |||
Lufteinlasstemperatur, °C | |||
Luftauslasstemperatur, °C |
|||
Dynamischer Luftdruck, mm. Wasser. Kunst. | |||
Überhöhter statischer Luftdruck, mm. Wasser. Kunst. |
|||
Luftdruck B, mm. rt. Kunst. |
|||
Spannung U, V |
Tabelle 1.3
Berechnungstabelle
Name der Mengen |
|
|||
Dynamische Förderhöhe, N/m2 | ||||
Durchschnittliche Vorlauftemperatur, °C |
Zielsetzung: Bestimmung der isobaren Wärmekapazität von Luft nach der Flow-Calorimeter-Methode.
Die Übung:
Bestimmen Sie experimentell die durchschnittliche volumetrische isobare Wärmekapazität von Luft.
Berechnen Sie auf der Grundlage der erhaltenen experimentellen Daten die durchschnittlichen isobaren Massen- und molaren Wärmekapazitäten sowie die durchschnittlichen Massen-, Volumen- und molaren Wärmekapazitäten von Luft.
Bestimmen Sie den Adiabatenexponenten für Luft.
Vergleichen Sie die erhaltenen Daten mit der Tabelle.
Schätzen Sie die Genauigkeit experimenteller Daten ab.
WICHTIGSTE BESTIMMUNGEN.
Wärmekapazität- eine Eigenschaft, die angibt, wie viel Wärme dem System zugeführt werden muss, um seine Temperatur um ein Grad zu ändern.
In dieser Formulierung hat die Wärmekapazität die Bedeutung eines umfangreichen Parameters, d.h. abhängig von der Menge der Materie im System.
In diesem Fall ist es unmöglich, die thermischen Eigenschaften verschiedener Materialien zu quantifizieren, indem man sie miteinander vergleicht. Ein für die Praxis viel aussagekräftigerer Parameter ist der sogenannte spezifische Wärme.
Spezifische Wärme gibt an, wie viel Wärme auf eine Mengeneinheit eines Stoffes gebracht werden muss, um ihn um ein Grad zu erwärmen.
Abhängig von den Einheiten, in denen die Menge eines Stoffes gemessen wird, gibt es:
spezifische Massenwärmekapazität (C). Im SI-System wird es in gemessen
 ;
;

Verschiedene Arten spezifischer Wärmekapazitäten sind miteinander verbunden:
 ,
,
wo  - jeweils spezifische Masse, volumetrische und molare Wärmekapazität;
- jeweils spezifische Masse, volumetrische und molare Wärmekapazität;
 - Gasdichte unter normalen physikalischen Bedingungen, kg/m 3 ;
- Gasdichte unter normalen physikalischen Bedingungen, kg/m 3 ;
 - Molmasse des Gases, kg/kmol;
- Molmasse des Gases, kg/kmol;
 - das Volumen von einem Kilomol eines idealen Gases unter normalen physikalischen Bedingungen.
- das Volumen von einem Kilomol eines idealen Gases unter normalen physikalischen Bedingungen.
Im Allgemeinen hängt die Wärmekapazität von der Temperatur ab, bei der sie bestimmt wird.
Die bei einem gegebenen Temperaturwert ermittelte Wärmekapazität, d.h. wenn die Temperaturänderung des Systems zu einem bestimmten Zeitpunkt gegen Null geht  , wird genannt wahre Wärmekapazität.
, wird genannt wahre Wärmekapazität.

Die Durchführung ingenieurtechnischer Berechnungen von Wärmeübertragungsprozessen wird jedoch stark vereinfacht, wenn man davon ausgeht, dass bei der Durchführung des Prozesses im Bereich der Systemtemperaturänderung aus  Vor
Vor  Die Wärmekapazität hängt nicht von der Temperatur ab und bleibt konstant. In diesem Fall ist die sog mittlere Wärmekapazität.
Die Wärmekapazität hängt nicht von der Temperatur ab und bleibt konstant. In diesem Fall ist die sog mittlere Wärmekapazität.
Durchschnittliche Wärmekapazität – die Wärmekapazität des Systems ist im Temperaturbereich konstant ab
– die Wärmekapazität des Systems ist im Temperaturbereich konstant ab  Vor
Vor  .
.

Die Wärmekapazität hängt von der Art des Prozesses der Wärmezufuhr zum System ab. Beim isobaren Prozess muss, um das System um ein Grad zu erwärmen, mehr Wärme zugeführt werden als beim isochoren Prozess. Dies ist darauf zurückzuführen, dass beim isobaren Prozess Wärme nicht nur für die Änderung der inneren Energie des Systems wie beim isochoren Prozess aufgewendet wird, sondern auch für die Durchführung der Volumenänderungsarbeit des Systems.
Dabei unterscheiden isobar und isochor
und isochor Wärmekapazität, und die isobare Wärmekapazität ist immer größer als die isochore. Die Beziehung zwischen diesen Arten von Wärmekapazitäten wird durch die Mayer-Formel bestimmt:
Wärmekapazität, und die isobare Wärmekapazität ist immer größer als die isochore. Die Beziehung zwischen diesen Arten von Wärmekapazitäten wird durch die Mayer-Formel bestimmt:

wo  - Gaskonstante, J/(kgGrad).
- Gaskonstante, J/(kgGrad).
Bei der praktischen Anwendung dieser Formel ist auf die Übereinstimmung der Größendimensionen zu achten  ,
, und
und  . In diesem Fall muss beispielsweise die spezifische Massenwärmekapazität verwendet werden. Diese Formel gilt auch für andere Arten von spezifischer Wärmekapazität, aber um Berechnungsfehler zu vermeiden, ist es immer notwendig, auf die Übereinstimmung zwischen den Dimensionen der in der Formel enthaltenen Größen zu achten. Zum Beispiel, wenn anstelle von verwendet wird
. In diesem Fall muss beispielsweise die spezifische Massenwärmekapazität verwendet werden. Diese Formel gilt auch für andere Arten von spezifischer Wärmekapazität, aber um Berechnungsfehler zu vermeiden, ist es immer notwendig, auf die Übereinstimmung zwischen den Dimensionen der in der Formel enthaltenen Größen zu achten. Zum Beispiel, wenn anstelle von verwendet wird  Universelle Gas Konstante
Universelle Gas Konstante  die Wärmekapazität muss spezifisch molar sein usw.
die Wärmekapazität muss spezifisch molar sein usw.
Bei einem isothermen Prozess wird die gesamte dem System zugeführte Wärme für externe Arbeit aufgewendet, und die interne Energie und folglich die Temperatur ändern sich nicht. Die Wärmekapazität des Systems bei einem solchen Prozess ist unendlich groß. In einem adiabatischen Prozess ändert sich die Temperatur des Systems ohne Wärmeaustausch mit der äußeren Umgebung, was bedeutet, dass die Wärmekapazität des Systems in einem solchen Prozess Null ist. Aus diesem Grund Es gibt keine Konzepte für isotherme oder adiabatische Wärmekapazität.
In dieser Arbeit wird das Durchflusskalorimeter-Verfahren zur Bestimmung der Wärmekapazität von Luft eingesetzt. Das Diagramm des Laboraufbaus ist in Abb. 1 dargestellt.

Abb.1. Schema des Laborständers
Dem Kalorimeter wird Luft durch einen Lüfter 1 zugeführt, der ein Rohr 2 aus einem Material mit geringer Wärmeleitfähigkeit und eine äußere Wärmeisolierung 3 ist, die notwendig ist, um einen Wärmeverlust an die Umgebung zu verhindern. Im Inneren des Kalorimeters befindet sich eine elektrische Heizung 4. Die Heizung wird über einen Spannungsregler 5 aus dem Wechselstromnetz gespeist. Die Leistung der elektrischen Heizung wird mit einem Wattmeter 6 gemessen. Zur Messung der Lufttemperatur am Einlass zum und Auslass aus dem Kalorimeter, Thermoelemente 7 werden verwendet, die über einen Schalter 8 mit dem Instrument zur Messung der Thermo-EMK 9 verbunden sind. Der Luftstrom durch das Kalorimeter wird durch den Regler 10 geändert und mit einem Schwimmerrotameter 11 gemessen.
REIHENFOLGE DER AUSFÜHRUNG DER ARBEIT.
Holen Sie sich die Anfangsdaten und die Erlaubnis des Leiters, die Arbeit auszuführen
Schalten Sie den Lüfter ein und stellen Sie den gewünschten Luftstrom ein.
Stellen Sie den gewünschten Wert für die Leistung der Elektroheizung ein.
Nach dem Aufbau eines stationären Temperaturregimes (gesteuert durch die Messwerte des Temperatursensors am Ausgang des Kalorimeters) werden die Lufttemperatur am Eingang und am Ausgang des Kalorimeters, der Luftstrom und die Heizleistung gemessen. Die Messergebnisse sind in der Tabelle der Versuchsdaten festgehalten (siehe Tabelle 1).
Tabelle 1.
Es wird ein neues Temperaturregime etabliert und es werden wiederholte Messungen durchgeführt. Messungen müssen in 2, 3 verschiedenen Modi durchgeführt werden.
Bringen Sie nach dem Ende der Messungen alle Regelorgane in ihren ursprünglichen Zustand und schalten Sie das Gerät aus.
Basierend auf den Messergebnissen wird der Wert der durchschnittlichen volumetrischen isobaren Wärmekapazität von Luft bestimmt:

wo  - die Wärmemenge, die der Luft im Kalorimeter zugeführt wird, W. Es wird gleich der elektrischen Leistung der Heizung genommen;
- die Wärmemenge, die der Luft im Kalorimeter zugeführt wird, W. Es wird gleich der elektrischen Leistung der Heizung genommen;
 - jeweils die Lufttemperatur am Ein- und Ausgang des Kalorimeters, K;
- jeweils die Lufttemperatur am Ein- und Ausgang des Kalorimeters, K;
 - volumetrischer Luftstrom durch das Kalorimeter, reduziert auf normale physikalische Bedingungen, m 3 / s;
- volumetrischer Luftstrom durch das Kalorimeter, reduziert auf normale physikalische Bedingungen, m 3 / s;
Um den Luftstrom durch das Kalorimeter auf Normalbedingungen zu bringen, wird die ideale Gaszustandsgleichung verwendet, die für normale physikalische Bedingungen und experimentelle Bedingungen geschrieben wurde:
 ,
,
wobei auf der linken Seite die Parameter der Luft am Kalorimetereinlass und auf der rechten Seite - unter normalen physikalischen Bedingungen.
Nach dem Finden der Werte  jeweils entsprechend
jeweils entsprechend  untersuchten Modi wird der Wert ermittelt
untersuchten Modi wird der Wert ermittelt  , die als Schätzung des experimentellen Werts der Wärmekapazität von Luft angenommen und in weiteren Berechnungen verwendet wird.
, die als Schätzung des experimentellen Werts der Wärmekapazität von Luft angenommen und in weiteren Berechnungen verwendet wird.

 , kJ/kg;
, kJ/kg;
Aus dem Verhältnis wird der Adiabatenindex für Luft ermittelt
 ;
;
Vergleichen Sie die erhaltenen Werte der isobaren und isochoren Wärmekapazität mit Tabellenwerten (siehe Anhang 1) und bewerten Sie die Genauigkeit der erhaltenen experimentellen Daten.
Tragen Sie die Ergebnisse in Tabelle 2 ein.
Tabelle 2.
TESTFRAGEN.
Was ist Wärmekapazität?
Welche Arten von spezifischer Wärmekapazität gibt es?
Was ist die durchschnittliche und wahre Wärmekapazität?
Was nennt man isobare und isochore Wärmekapazität? Wie hängen sie zusammen?
Welche der beiden Wärmekapazitäten ist größer: C p oder C v und warum? Geben Sie eine Erklärung anhand des 1. Hauptsatzes der Thermodynamik.
Merkmale der praktischen Anwendung der Mayer-Formel?
Warum gibt es die Konzepte der isothermen und adiabatischen Wärmekapazität nicht?
Anhang 1.
Wärmekapazität der Luft in Abhängigkeit von der Temperatur
|
|
|
|
|
|
| ||
UNTERSUCHUNG DES PROZESSES DES ADIABATISCHEN GASABFLUSSES DURCH EINE UMKEHRDÜSE.
Zielsetzung: experimentelle und theoretische Untersuchung der thermodynamischen Eigenschaften des Prozesses des Gasaustritts aus einer konvergierenden Düse.
Die Übung:
1. Ermitteln Sie für ein gegebenes Gas die Abhängigkeit der tatsächlichen Ausströmgeschwindigkeit und Durchflussmenge von der vorhandenen Druckdifferenz vor und nach der Düse.
WICHTIGSTE BESTIMMUNGEN.
Die thermodynamische Untersuchung der Prozesse der Gasbewegung durch Kanäle ist von großer praktischer Bedeutung. Die wesentlichen Bestimmungen der Theorie des Gasaustritts werden bei der Berechnung des Strömungsweges von Dampf- und Gasturbinen, Strahltriebwerken, Kompressoren, pneumatischen Antrieben und vielen anderen technischen Systemen verwendet.
Ein Kanal mit veränderlichem Querschnitt, durch den sich der Gasstrom mit abnehmendem Druck und zunehmender Geschwindigkeit ausdehnt, wird als Kanal bezeichnet Düse. In den Düsen wird die potentielle Energie des Gasdrucks in die kinetische Energie der Strömung umgewandelt. Wenn im Kanal der Druck des Arbeitsmediums zunimmt und die Geschwindigkeit seiner Bewegung abnimmt, wird ein solcher Kanal genannt Diffusor. Bei Diffusoren erfolgt die Erhöhung der potentiellen Energie des Gases durch Verringerung seiner kinetischen Energie.
Zur Vereinfachung der theoretischen Beschreibung des Gasausströmvorgangs werden folgende Annahmen getroffen:
das Gas ist ideal;
es gibt keine innere Reibung im Gas, d.h. Viskosität;
es gibt keine irreversiblen Verluste im Ablaufprozess;
der Gasstrom ist stetig und stationär, d.h. an jedem Punkt des Strömungsquerschnitts sind die Strömungsgeschwindigkeit w und die Gaszustandsparameter (p, v, T) gleich und ändern sich nicht mit der Zeit;
die Strömung ist eindimensional, d.h. Strömungsverhalten ändert sich nur in Strömungsrichtung;
es findet kein Wärmeaustausch zwischen der Strömung und der äußeren Umgebung statt, d.h. der Ausflussprozess ist adiabat.
Die theoretische Beschreibung des Gasausströmvorgangs basiert auf den folgenden Gleichungen.
Ideale Gaszustandsgleichung
 ,
,
wobei R die Gaskonstante ist;
T ist die absolute Temperatur des Gasstroms.
Adiabatische Gleichung (Poisson-Gleichung)

wobei p der absolute Gasdruck ist;
k ist der Adiabatenexponent.
Strömungskontinuitätsgleichung

wobei F die Querschnittsfläche der Strömung ist;
w ist die Durchflussrate;
v ist das spezifische Gasvolumen.
Bernoulli-Gleichung für ein kompressibles Arbeitsmedium unter Berücksichtigung des Fehlens innerer Reibung

Diese Gleichung zeigt, dass mit zunehmendem Druck eines Gases seine Geschwindigkeit und kinetische Energie immer abnehmen und umgekehrt mit abnehmendem Druck die Geschwindigkeit und kinetische Energie eines Gases zunehmen.
Die Gleichung des 1. Hauptsatzes der Thermodynamik für die Strömung.
Der 1. Hauptsatz der Thermodynamik hat im allgemeinen Fall folgende Form
 ,
,
wo  ist die elementare Wärmemenge, die dem System zugeführt wird;
ist die elementare Wärmemenge, die dem System zugeführt wird;
 ist eine elementare Änderung der inneren Energie des Systems;
ist eine elementare Änderung der inneren Energie des Systems;
 ist die elementare Volumenänderungsarbeit des Systems.
ist die elementare Volumenänderungsarbeit des Systems.
Bei einem beweglichen thermodynamischen System (Strömung eines bewegten Gases) wird ein Teil der Volumenänderungsarbeit für die Überwindung der äußeren Druckkräfte aufgewendet, d.h. für den Gastransport. Dieser Teil der Gesamtarbeit heißt schiebende Arbeit. Die restliche Arbeit der Volumenänderung kann sinnvoll genutzt werden, beispielsweise um das Turbinenrad zu drehen. Dieser Teil des Gesamtbetriebs des Systems wird genannt verfügbare oder technische Arbeit.
Im Falle einer Gasströmung besteht die Volumenänderungsarbeit also aus 2 Begriffen - der Schubarbeit und der technischen (verfügbaren) Arbeit:

wo  - elementare Schiebearbeiten;
- elementare Schiebearbeiten;
 - elementare technische Arbeiten
- elementare technische Arbeiten
Dann hat der 1. Hauptsatz der Thermodynamik für die Strömung die Form
 ,
,
wo  - elementare Änderung der Enthalpie des Systems.
- elementare Änderung der Enthalpie des Systems.
Bei adiabatischer Abströmung
Also bei adiabatischer Ausfluss, technische Arbeit wird durch den Verlust der Gasenthalpie verrichtet.
Basierend auf den obigen Annahmen für den Fall des Gasaustritts aus einem Behälter mit unbegrenztem Fassungsvermögen (in diesem Fall die anfängliche Gasgeschwindigkeit  ) Formeln zur Bestimmung der theoretischen Geschwindigkeit erhalten
) Formeln zur Bestimmung der theoretischen Geschwindigkeit erhalten  und Gasmassenstrom
und Gasmassenstrom  im Austrittsbereich der Düse:
im Austrittsbereich der Düse:
 oder
oder


wo  - Druck und Temperatur des Gases im Einlassbereich der Düse;
- Druck und Temperatur des Gases im Einlassbereich der Düse;
 - spezifische Enthalpie der Strömung jeweils am Düseneinlass und Düsenauslass;
- spezifische Enthalpie der Strömung jeweils am Düseneinlass und Düsenauslass;
 - adiabatischer Index;
- adiabatischer Index;
 - Gaskonstante;
- Gaskonstante;
 - das Verhältnis der Drücke am Auslass der Düse und am Einlass der Düse;
- das Verhältnis der Drücke am Auslass der Düse und am Einlass der Düse;
 - Bereich des Auslassabschnitts der Düse.
- Bereich des Auslassabschnitts der Düse.
Eine Analyse der erhaltenen Formeln zeigt, dass nach der anerkannten Theorie die Abhängigkeiten der theoretischen Geschwindigkeit und des Massenstroms vom Druckverhältnis die Form haben sollten, die in den Diagrammen durch die mit dem Buchstaben T gekennzeichneten Kurven dargestellt wird (siehe Abb. 1 und Abb. 2). Aus den Diagrammen folgt, dass nach der Theorie, wenn die Werte von von 1 auf 0 abnehmen, die Abgasgeschwindigkeit kontinuierlich zunehmen sollte (siehe Abb. 1), und der Massendurchsatz zunächst auf einen bestimmten Maximalwert ansteigt , und sollte dann bei = 0 auf 0 abnehmen (siehe Abb.2).

Bild 1. Abhängigkeit der Abflussmenge vom Druckverhältnis

Abb. 2. Abhängigkeit des Massenstroms vom Druckverhältnis
Bei einer experimentellen Untersuchung des Ausströmens von Gasen aus einer konvergierenden Düse wurde jedoch festgestellt, dass bei einer Verringerung von von 1 auf 0 die tatsächliche Ausströmgeschwindigkeit und dementsprechend die tatsächliche Durchflussrate zunächst in voller Übereinstimmung mit dem Akzeptierten zunehmen Theorie des Prozesses, aber nach Erreichen des Maximums bleiben ihre Werte bei einer weiteren Abnahme von bis auf 0 unverändert
Die Art dieser Abhängigkeiten wird in den Diagrammen durch mit dem Buchstaben D gekennzeichnete Kurven dargestellt (siehe Abb. 1 und Abb. 2).
Eine physikalische Erklärung für die Diskrepanz zwischen der theoretischen Abhängigkeit und experimentellen Daten wurde erstmals 1839 von dem französischen Wissenschaftler Saint-Venant vorgeschlagen. Dies wurde durch weitere Untersuchungen bestätigt. Es ist bekannt, dass sich jede, selbst eine schwache Störung eines stationären Mediums mit Schallgeschwindigkeit darin ausbreitet. Bei einer Strömung, die sich durch eine Düse in Richtung der Störungsquelle bewegt, ist die Übertragungsrate der Störung in die Düse, d. h. entgegen der Strömungsrichtung um den Wert der Strömungsgeschwindigkeit selbst geringer sein. Dies ist die sogenannte relative Ausbreitungsgeschwindigkeit der Störung, die gleich ist  . Beim Passieren der Störwelle innerhalb der Düse entlang der gesamten Strömung kommt es zu einer entsprechenden Druckumverteilung, deren Ergebnis laut Theorie eine Erhöhung der Ausströmgeschwindigkeit und des Gasflusses ist. Bei konstantem Gasdruck am Düseneintritt P 1 = const entspricht eine Abnahme des Drucks des Mediums, in das das Gas strömt, einer Abnahme des Wertes von β.
. Beim Passieren der Störwelle innerhalb der Düse entlang der gesamten Strömung kommt es zu einer entsprechenden Druckumverteilung, deren Ergebnis laut Theorie eine Erhöhung der Ausströmgeschwindigkeit und des Gasflusses ist. Bei konstantem Gasdruck am Düseneintritt P 1 = const entspricht eine Abnahme des Drucks des Mediums, in das das Gas strömt, einer Abnahme des Wertes von β.
Wenn jedoch der Druck des Mediums, in das das Gas strömt, auf einen bestimmten Wert sinkt, bei dem die Ausströmgeschwindigkeit am Düsenaustritt gleich der örtlichen Schallgeschwindigkeit wird, kann sich die Störwelle nicht innerhalb der Düse ausbreiten, da die Relativgeschwindigkeit seiner Ausbreitung im Medium in der der Bewegung entgegengesetzten Richtung gleich Null ist:
 .
.
In dieser Hinsicht kann die Druckumverteilung in der Strömung entlang der Düse nicht auftreten, und die Gasausströmungsgeschwindigkeit am Düsenausgang bleibt unverändert und gleich der lokalen Schallgeschwindigkeit. Mit anderen Worten, die Strömung „bläst“ die von außen erzeugte Verdünnung sozusagen aus der Düse heraus. Auch wenn der Absolutdruck des Mediums hinter der Düse nicht weiter abnimmt, steigt die Ausströmgeschwindigkeit und damit die Durchflussmenge nicht weiter an, weil bildlich gesprochen, so Reynolds, "hört die Düse auf zu spüren, was außerhalb passiert" oder, wie sie manchmal sagen, "die Düse ist verriegelt". Eine Analogie zu diesem Phänomen ist die Situation, die manchmal beobachtet werden kann, wenn der Klang der Stimme einer Person von einem starken Gegenwind weggeblasen wird und der Gesprächspartner seine Worte nicht hören kann, selbst wenn er sehr nah ist, wenn der Wind von ihm in Richtung des Windes weht Lautsprecher.
Der Ausströmmodus, bei dem die Ausströmgeschwindigkeit am Düsenaustritt die örtliche Schallgeschwindigkeit erreicht, wird bezeichnet Kritischer Modus. Ablaufrate  , Verbrauch
, Verbrauch  und Druckverhältnis
und Druckverhältnis  entsprechend diesem Modus werden auch aufgerufen kritisch. Dieses Regime entspricht den Maximalwerten der Durchflussmenge und Durchflussmenge, die erreicht werden können, wenn das Gas durch eine herkömmliche konvergierende Düse strömt. Das kritische Druckverhältnis wird durch die Formel bestimmt
entsprechend diesem Modus werden auch aufgerufen kritisch. Dieses Regime entspricht den Maximalwerten der Durchflussmenge und Durchflussmenge, die erreicht werden können, wenn das Gas durch eine herkömmliche konvergierende Düse strömt. Das kritische Druckverhältnis wird durch die Formel bestimmt
 ,
,
wobei k der adiabatische Exponent ist.
Das kritische Druckverhältnis hängt nur von der Art des Gases ab und ist für ein bestimmtes Gas konstant. Zum Beispiel:
für einatomige Gase k= 1,66 und bis 0,489;
für 2 atomare Gase und Luft k= 1,4 und bis 0,528
für 3 und mehratomige Gase k=1,3 und bis 0,546.
Die im Rahmen der angenommenen Annahmen erhaltenen theoretischen Abhängigkeiten zur Bestimmung der Ausströmgeschwindigkeit und des Gasdurchflusses sind somit tatsächlich nur im Wertebereich gültig  . Für Werte
. Für Werte  die Durchflussrate und der Durchfluss bleiben für gegebene Bedingungen tatsächlich konstant und maximal.
die Durchflussrate und der Durchfluss bleiben für gegebene Bedingungen tatsächlich konstant und maximal.
Darüber hinaus gelten für reale Strömungsverhältnisse die tatsächliche Ausströmgeschwindigkeit und Gasdurchflussmenge am Düsenaustritt auch bei den Werten  etwas niedriger sein als ihre entsprechenden theoretischen Werte. Dies liegt an der Reibung des Strahls an den Wänden der Düse. Die Temperatur am Ausgang der Düse ist etwas höher als die theoretische Temperatur. Dies liegt daran, dass ein Teil der verfügbaren Arbeit des Gasstroms abgeführt und in Wärme umgewandelt wird, was zu einer Temperaturerhöhung führt.
etwas niedriger sein als ihre entsprechenden theoretischen Werte. Dies liegt an der Reibung des Strahls an den Wänden der Düse. Die Temperatur am Ausgang der Düse ist etwas höher als die theoretische Temperatur. Dies liegt daran, dass ein Teil der verfügbaren Arbeit des Gasstroms abgeführt und in Wärme umgewandelt wird, was zu einer Temperaturerhöhung führt.
BESCHREIBUNG DES LABORSTÄNDERS.
Die Untersuchung des Prozesses des Gasaustritts aus der Düse wird an einer Anlage durchgeführt, die auf der Methode der Simulation realer physikalischer Prozesse basiert. Die Installation besteht aus einem PC, der mit einem Modell des Arbeitsbereichs verbunden ist, einem Bedienfeld und Messgeräten. Das Installationsdiagramm ist in Abb. 3 dargestellt.

Abb. 3. Schema einer Anlage zur Untersuchung des Prozesses des Gasaustritts
Der Arbeitsabschnitt der Anlage ist ein Rohr, in dem die untersuchte konvergierende Düse 3 mit einem Austrittsdurchmesser d = 1,5 mm eingebaut ist. Der Gasstrom (Luft, Kohlendioxid (CO 2 ), Helium (He)) durch die Düse wird mit Hilfe einer Vakuumpumpe 5 erzeugt. Der Gasdruck am Einlass ist gleich dem barometrischen Druck (P 1 = B). Der Gasdurchfluss G und der Durchfluss w werden durch das Ventil 4 geregelt. Die Betriebsarten werden durch den Unterdruck hinter der Düse P 3 bestimmt, der auf einer Digitalanzeige 6 erfasst wird. Der Gasdurchfluss wird mit einer Messmembran mit einem Durchmesser d d = 5 gemessen mm. Der Druckabfall über der Membrane H wird am Digitalanzeiger 7 aufgezeichnet und auf dem PC-Monitor dupliziert. Die Verdünnung P 2 im Auslaufbereich der Düse wird ebenfalls auf der Digitalanzeige 6 und auf dem Bildschirm erfasst. Als Ergebnis der Kalibrierung wird der Durchflusskoeffizient der Messmembran mit kalibrierter Bohrung = 0,95 ermittelt.
REIHENFOLGE DER AUSFÜHRUNG DER ARBEIT.
Verbinden Sie die Anlage mit dem Netzwerk, treten Sie in einen Dialog mit dem im Computer eingebetteten Experimentprogramm.
Wählen Sie die Gasart für das Experiment aus.
Schalten Sie die Vakuumpumpe ein. Dadurch entsteht hinter dem Ventil 4 ein Unterdruck, der auf dem Bildschirm angezeigt wird.
Durch allmähliches Öffnen des Ventils 4 wird das Mindestvakuum eingestellt
P 3 = 0,1 atm, was dem 1. Modus entspricht. Dies startet den Gasfluss.
Tragen Sie in das Versuchsprotokoll (Tabelle 1) die Zahlenwerte P 3 ,P 2 ,H ein, die mit Hilfe der Digitalanzeigen 6 und 7 festgelegt wurden.
Messungen der Werte P 2 ,H für nachfolgende Modi durchführen, die den Werten des von der Vakuumpumpe erzeugten Vakuums entsprechen,
P 3 = 0,2; 0,3; 0,4; 0,5…..0,9 at. Trage die Messergebnisse in Tabelle 1 ein
Tabelle 1.
Gasdruck am Düseneintritt P 1 =B= Pa.
Die Gastemperatur am Düseneintritt t 1 =C.
|
Modus Nr. |
Messergebnisse |
|||
VERARBEITUNG DER MESSERGEBNISSE.
Es wird der Absolutdruck des Mediums P 3 hinter der Düse bestimmt, in die das Gas ausströmt
 , Pa
, Pa
4.2. Der absolute Gasdruck P 2 im Austrittsabschnitt der Düse wird ermittelt
 , Pa
, Pa
Der tatsächliche Gasmassenstrom wird durch die Größe des Druckabfalls H über der Messmembran bestimmt
 , kg/s
, kg/s
wo  - Durchfluss der Messmembran;
- Durchfluss der Messmembran;
 - Druckabfall über der Messmembran, Pa;
- Druckabfall über der Messmembran, Pa;
 - Gasdichte, kg/m 3 ;
- Gasdichte, kg/m 3 ;
 - barometrischer Druck, Pa;
- barometrischer Druck, Pa;
 - Gaskonstante, J/(kg∙deg);
- Gaskonstante, J/(kg∙deg);
 - Gastemperatur, С;
- Gastemperatur, С;
 - Durchmesser der Messöffnung.
- Durchmesser der Messöffnung.
4.4. Da der Ausströmvorgang adiabat ist, wird die theoretische Gastemperatur T 2 am Düsenaustritt mit der bekannten Beziehung für den adiabaten Vorgang bestimmt:

4.5. Die tatsächliche Geschwindigkeit des Ablaufs wird bestimmt  und Gastemperatur
und Gastemperatur  im Austrittsbereich der Düse
im Austrittsbereich der Düse
 , Frau;
, Frau;
wo  - tatsächlicher Massendurchsatz des Gases, kg/s;
- tatsächlicher Massendurchsatz des Gases, kg/s;
 - Temperatur (K) bzw. Druck (Pa) des Gases im Austrittsbereich der Düse;
- Temperatur (K) bzw. Druck (Pa) des Gases im Austrittsbereich der Düse;

 - Bereich des Auslassabschnitts der Düse;
- Bereich des Auslassabschnitts der Düse;
 - Durchmesser des Auslassabschnitts der Düse.
- Durchmesser des Auslassabschnitts der Düse.
Andererseits basiert auf dem 1. Hauptsatz der Thermodynamik für die Strömung
wo  - spezifische Enthalpie des Gases jeweils am Einlass und Auslass der Düse, J/kg;
- spezifische Enthalpie des Gases jeweils am Einlass und Auslass der Düse, J/kg;
 - Gastemperatur am Einlass bzw. Auslass der Düse, K;
- Gastemperatur am Einlass bzw. Auslass der Düse, K;
 - spezifische isobare Wärmekapazität von Gas, J/(kgGrad);
- spezifische isobare Wärmekapazität von Gas, J/(kgGrad);
Durch Gleichsetzen der rechten Seiten der Gleichungen (17) und (18) und Auflösen der resultierenden quadratischen Gleichung für T 2 wird die tatsächliche Gastemperatur im Auslassabschnitt der Düse bestimmt.

 oder
oder
 ,
,
wo  ;
;
 ;
;
 .
.
4.6. Es wird der theoretische Massenstrom des Gases beim adiabatischen Ausströmen bestimmt

 , kg/s;
, kg/s;
wo  - Fläche des Auslassabschnitts der Düse, m 2 ;
- Fläche des Auslassabschnitts der Düse, m 2 ;

 - absoluter Gasdruck am Düseneinlass, Pa;
- absoluter Gasdruck am Düseneinlass, Pa;
 - Gastemperatur am Düseneinlass, K;
- Gastemperatur am Düseneinlass, K;
 - Gaskonstante, J/(kgGrad);
- Gaskonstante, J/(kgGrad);
 ist der adiabatische Index.
ist der adiabatische Index.
4.7. Der theoretische Gasdurchsatz wird ermittelt

wo  - Gastemperatur im Einlassbereich der Düse;
- Gastemperatur im Einlassbereich der Düse;
 - adiabatischer Index;
- adiabatischer Index;
 - Gaskonstante;
- Gaskonstante;
 - Druckverhältnis;
- Druckverhältnis;
 - absoluter Druck des Mediums, in das Gas ausströmt, Pa;
- absoluter Druck des Mediums, in das Gas ausströmt, Pa;
 - absoluter Gasdruck am Düseneintritt, Pa.
- absoluter Gasdruck am Düseneintritt, Pa.
4.8. Der maximale theoretische Gasdurchsatz wird ermittelt  (Abfluss ins Leere bei P 3 = 0) und lokale theoretische Schallgeschwindigkeit (kritische Geschwindigkeit)
(Abfluss ins Leere bei P 3 = 0) und lokale theoretische Schallgeschwindigkeit (kritische Geschwindigkeit)  .
.


4.9. Die Berechnungsergebnisse sind in Tabelle 2 eingetragen.
Tabelle 2.
|
Berechnungsergebnisse |
||||||||||
4.10. In Koordinaten  und
und  Abhängigkeitsgraphen werden erstellt, und ein Abhängigkeitsgraph wird ebenfalls erstellt
Abhängigkeitsgraphen werden erstellt, und ein Abhängigkeitsgraph wird ebenfalls erstellt  . Die Diagramme bestimmen den Wert des kritischen Druckverhältnisses
. Die Diagramme bestimmen den Wert des kritischen Druckverhältnisses  ,
,
die mit der berechneten verglichen wird
 .
.
4.11. Ziehen Sie auf der Grundlage der Ergebnisse von Berechnungen und grafischen Konstruktionen eine Schlussfolgerung über Folgendes:
Wie hängen die theoretische Ausströmgeschwindigkeit und der Gasdurchsatz vom Druckverhältnis β ab?
Wie hängen die tatsächliche Ausströmgeschwindigkeit und der Gasdurchfluss vom Druckverhältnis β ab?
Warum sind die Werte der tatsächlichen Ausströmgeschwindigkeit und des Gasdurchflusses bei gleichen äußeren Bedingungen geringer als die entsprechenden theoretischen Werte?
TESTFRAGEN.
Welche Annahmen werden bei der theoretischen Beschreibung der Thermodynamik des Gasausströmvorgangs getroffen?
Mit welchen Grundgesetzen wird der Abflussprozess theoretisch beschrieben?
Aus welchen Komponenten besteht die Arbeit, die der Gasstrom beim Durchströmen der Düse verrichtet?
In welchem Zusammenhang stehen Enthalpie und technische Arbeit einer Gasströmung bei adiabatischer Abströmung?
Was ist ein kritisches Strömungsregime und wie wird es charakterisiert?
Wie lässt sich aus physikalischer Sicht die Diskrepanz zwischen der theoretischen und experimentellen Abhängigkeit der Ausströmgeschwindigkeit und der Strömungsgeschwindigkeit von erklären?
Wie wirken sich die tatsächlichen Ausströmbedingungen auf Geschwindigkeit, Durchfluss und Temperatur des Gases am Düsenaustritt aus?
Luftfeuchtigkeit. Wärmekapazität und Enthalpie der Luft
Atmosphärische Luft ist ein Gemisch aus trockener Luft und Wasserdampf (von 0,2 % bis 2,6 %). Somit kann die Luft fast immer als feucht angesehen werden.
Die mechanische Mischung aus trockener Luft und Wasserdampf heißt feuchte Luft oder Luft/Dampf-Gemisch. Der maximal mögliche Gehalt an dampfförmiger Feuchtigkeit in der Luft m wie temperaturabhängig t und Druck P Mischungen. Wenn es sich ändert t und P die Luft kann von anfänglich ungesättigt in einen mit Wasserdampf gesättigten Zustand übergehen, und dann beginnt überschüssige Feuchtigkeit in Form von Nebel, Raureif oder Schnee im Gasvolumen und auf den umschließenden Oberflächen auszufallen.
Die Hauptparameter, die den Zustand feuchter Luft charakterisieren, sind: Temperatur, Druck, spezifisches Volumen, Feuchtigkeitsgehalt, absolute und relative Feuchtigkeit, Molekulargewicht, Gaskonstante, Wärmekapazität und Enthalpie.
Nach dem Daltonschen Gesetz für Gasgemische Gesamtdruck feuchter Luft (P) ist die Summe der Partialdrücke von trockener Luft P c und Wasserdampf P p: P \u003d P c + P p.
Ebenso werden das Volumen V und die Masse m feuchter Luft durch die Beziehungen bestimmt:
V \u003d V c + V p, m \u003d m c + m p.
Dichte und spezifisches Volumen feuchter Luft (v) definiert:
![]()
Molekulargewicht feuchter Luft:
![]()
wobei B der barometrische Druck ist.
Da die Luftfeuchtigkeit während des Trocknungsprozesses kontinuierlich zunimmt und die Menge an trockener Luft im Dampf-Luft-Gemisch konstant bleibt, wird der Trocknungsprozess danach beurteilt, wie sich die Menge an Wasserdampf pro 1 kg trockener Luft ändert, und alle Indikatoren von das Dampf-Luft-Gemisch (Wärmekapazität, Feuchtigkeitsgehalt, Enthalpie usw.) bezieht sich auf 1 kg trockene Luft in feuchter Luft.
d \u003d m p / m c, g / kg oder X \u003d m p / m c.
Absolute Luftfeuchtigkeit- Dampfmasse in 1 m 3 feuchter Luft. Dieser Wert ist numerisch gleich .
Relative Luftfeuchtigkeit - ist das Verhältnis der absoluten Feuchtigkeit ungesättigter Luft zur absoluten Feuchtigkeit gesättigter Luft unter gegebenen Bedingungen:
hier , häufiger wird jedoch die relative Luftfeuchtigkeit in Prozent angegeben.
Für die Dichte feuchter Luft gilt die Beziehung:
Spezifische Wärme feuchte Luft:
c \u003d c c + c p × d / 1000 \u003d c c + c p × X, kJ / (kg × ° С),
wobei c c die spezifische Wärmekapazität trockener Luft ist, c c = 1,0;
c p - spezifische Wärmekapazität von Dampf; mit n = 1,8.
Die Wärmekapazität trockener Luft bei konstantem Druck und kleinen Temperaturbereichen (bis 100 ° C) für ungefähre Berechnungen kann als konstant angesehen werden und beträgt 1,0048 kJ / (kg × ° C). Für überhitzten Dampf kann die mittlere isobare Wärmekapazität bei Atmosphärendruck und geringen Überhitzungsgraden ebenfalls als konstant und gleich 1,96 kJ/(kg×K) angenommen werden.
Enthalpie (i) von feuchter Luft- Dies ist einer seiner Hauptparameter, der bei Berechnungen von Trocknungsanlagen häufig verwendet wird, hauptsächlich um die Wärme zu bestimmen, die für die Verdunstung von Feuchtigkeit aus den zu trocknenden Materialien aufgewendet wird. Die Enthalpie feuchter Luft wird auf ein Kilogramm trockener Luft in einem Dampf-Luft-Gemisch bezogen und ist definiert als die Summe der Enthalpien von trockener Luft und Wasserdampf, also
ich \u003d ich c + ich p × X, kJ / kg.
Bei der Berechnung der Enthalpie von Gemischen muss der Startbezugspunkt für die Enthalpien aller Komponenten gleich sein. Für Berechnungen von feuchter Luft kann davon ausgegangen werden, dass die Enthalpie von Wasser bei 0 ° C Null ist, dann wird die Enthalpie von trockener Luft auch ab 0 ° C gezählt, dh i in \u003d c in * t \u003d 1,0048 t.