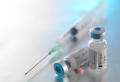
Faze metode fluorescentne in situ hibridizacije. FISH je študija za diferencialno diagnozo. FISH je postal široko dostopen
Metoda določanja fluorescenčna in situ hibridizacija.
Material v študiji Glej v opisu
Možnost obiska na domu
Študija se uporablja za izbiro posamezne adjuvantne kemoterapije za raka dojke ali raka želodca.
Rak dojke (BC) je na prvem mestu med onkološkimi boleznimi pri ženskah. Tumorske celice dojke lahko vsebujejo različne vrste receptorjev, ki so občutljivi na določene snovi (hormone ali druge biološko aktivne molekule). Glede na prisotnost hormonskih receptorjev (estrogena in progesterona) ali receptorja za človeški epidermalni rastni faktor tipa 2 (Human Epidermal Growth Factor Receptor 2, HER2) v tumorskih celicah ločimo hormonsko-receptorsko pozitiven, HER2-pozitiven in trojno negativen rak dojke. . To je pomembno upoštevati pri individualnem izboru terapije in za napoved uspeha zdravljenja.
HER2 je receptor, ki je prisoten v tkivih in normalno sodeluje pri regulaciji celične delitve in diferenciacije. Njegov presežek na površini tumorskih celic (hiperekspresija) določa hitro nenadzorovano rast neoplazme, visoko tveganje za metastaze in nizko učinkovitost nekaterih vrst zdravljenja. Hiperekspresija HER2 pri nekaterih podtipih raka dojke vodi do povečane proliferacije in angiogeneze ter do disregulacije apoptoze (gensko programirano samouničenje celic). Trenutno obstajajo zdravila, ki ciljajo na receptor HER2. To je zlasti Herceptin (trastuzumab), ki je monoklonsko protitelo proti receptorjem HER2/neu.
Amplifikacija in prekomerna ekspresija onkogena HER2 (ErbB-2) sta razmeroma specifična dogodka za karcinom dojke in se praktično ne pojavljata pri tumorjih drugih lokalizacij. Rak želodca (GC) je ena redkih izjem: aktivacija HER2 je opažena v približno 10-15% primerov malignih novotvorb tega organa in je povezana z agresivnim potekom bolezni. Pri HER2-pozitivnem raku dojke je lahko na površini tumorskih celic prisoten presežek receptorjev HER2 (ki jih imenujemo HER2 pozitivni ali Hercept pozitivni). Ta pojav opazimo pri 15-20% žensk z rakom dojke. Ocena statusa HER2 je pomembna za določitev taktike zdravljenja.
Glavni standardizirani metodi za odkrivanje čezmerne ekspresije HER2/neu in/ali pomnoževanja gena HER2/neu sta imunohistokemična (IHC) metoda in fluorescenčna in situ hibridizacija (FISH). Obe študiji se izvajata na histoloških preparatih (odseki tumorskega materiala, vdelani v parafin) z uporabo poliklonskih protiteles (IHC), fluorescenčnih sond (FISH) in različnih slikovnih sistemov.
Pri vrednotenju rezultatov IHC reakcije se izražanje upošteva le v invazivni komponenti tumorja. Rezultati reakcije so ovrednoteni s točkovno lestvico: 0, 1+, 2+, 3+, ki jo je razvil proizvajalec testa in odobrili strokovnjaki. Status Hercepta, ocenjen kot 0 in 1+, je treba obravnavati kot negativnega - ni prekomerne ekspresije proteina, kar je v korelaciji z odsotnostjo pomnoževanja njegovega gena. Herceptov status, ocenjen kot 3+, je pozitiven, kar pomeni, da je prisotna prekomerna ekspresija beljakovin, kar je v korelaciji s prisotnostjo pomnoževanja gena. Herceptov status 2+ se šteje za nedoločen, to pomeni, da izražanja beljakovin, določenega na podlagi imunohistokemične reakcije, ni mogoče zanesljivo oceniti glede pomnoževanja gena, zato je potrebna študija, ki neposredno razkrije prisotnost ali odsotnost pomnoževanja. Metoda FISH se uporablja na rezih iz istega vzorca (bloka), na katerem je bila opravljena imunohistokemična študija. Pri hibridizaciji FISH se prisotnost pomnoževanja gena HER2 oceni s štetjem razmerja med rdečimi fluorescentnimi (ki ustrezajo označenim genom HER2) in zelenimi fluorescentnimi signali, ki označujejo centromerno regijo 17. kromosoma. Razmerje, večje od 2, kaže na prisotnost ojačanja HER2. Metoda FISH je občutljivejša od IHC, saj omogoča neposredno oceno prisotnosti ali odsotnosti pomnoževanja.
Material za raziskavo: parafinski blok z biopsijo tumorja.
Pozor! OBVEZNO:
- stekelca z IHC-barvanjem s protitelesi proti HER2/neu
- napotnico zdravnika ali izpisek z rezultati histološke in IHC študije s protitelesi proti Her-2/neu
Literatura
- Zavalishina L.E., Frank G.A. Morfološka študija statusa HER2. Metodologija in atlas. - M.: Ed. Media Medica. 2006:98.
- Maligne bolezni v Rusiji v letu 2011 (obolevnost in umrljivost). Ed. V IN. Chissova, V.V. Starinsky, G.V. Petrova. - M .: FGBU "MNIOI jim. P.A. Herzen" Ministrstva za zdravje Rusije. 2013: 289.
- Onkologija. Klinične smernice. Združenje onkologov Rusije. Ed. V IN. Chissova, S.L. Darjalova. - M.: Ed. "GEOTAR-Media". 2008: 702.
- Bang Y.J., Van Cutsem E., Feyereislova A., Chung H.C., Shen L., Sawaki A. et al. Trastuzumab v kombinaciji s kemoterapijo v primerjavi s samo kemoterapijo za zdravljenje HER2-pozitivnega napredovalega raka želodca ali gastroezofagealnega spoja (ToGA): odprto, randomizirano kontrolirano preskušanje faze 3. Lanceta. 2010;376:687-697.
- Dabbs D.J. Diagnostična imunohistokemija: Teranostične in genomske aplikacije. Elsevier, 4. izdaja. 2013: 960.
- Ferlay J., Shin H.R., Bray F., Forman D., Mathers C., Parkin D.M. GLOBOCAN 2008, Incidenca raka in umrljivost po vsem svetu: IARC Cancer Base št. 10. Lyon, Francija: Mednarodna agencija za raziskave raka; 2010. Dostopno na: http://globocan.iarc.fr.
- Goldhirsch A., Glick J.H., Gelber R.D., Coates A.S., Thurlimann B., Senn H.J. Poudarki srečanja: Mednarodno strokovno soglasje o primarni terapiji zgodnjega raka dojke 2005. Annals of Oncology. 2005;16(10):1569-1583.
- Kurman R.J., Carcangiu M.L., Herrington C.S., Young R.H. Klasifikacija WHO tumorjev ženskih reproduktivnih organov. WHO Press, 4. izdaja. 2014; 4: 316.
- NordiQC. http://www.nordiqc.org.
- Park D.I., Yun J.W., Park J.H. et al. Povečanje Her2/neu je neodvisen prognostični dejavnik pri raku želodca. Prebavne bolezni in znanosti. 2006;51(8):1371-1379.
- Slamon D. et al. Adjuvant Trastuzumab pri HER2-pozitivnem raku dojke. New England Journal of Medicine. 2011;365:1273-1283.
- Fluorescenčna in situ hibridizacija ali metoda FISH (fluorescence in situ hybridization – FISH) je citogenetska metoda, ki se uporablja za detekcijo in določanje položaja specifičnega zaporedja DNA na metafaznih kromosomih ali v interfaznih jedrih in situ. Poleg tega se FISH uporablja za odkrivanje specifičnih mRNA v vzorcu tkiva. V slednjem primeru metoda FISH omogoča ugotavljanje prostorsko-časovnih značilnosti izražanja genov v celicah in tkivih.
Metoda FISH se uporablja v predimplantacijski, prenatalni in postnatalni genetski diagnostiki, pri diagnostiki onkoloških bolezni, pri retrospektivni biološki dozimetriji.
Sorodni pojmi
Mikronukleus - v citologiji delček jedra v evkariontski celici, ki ne vsebuje celotnega genoma, potrebnega za njeno preživetje. Je patološka struktura in jo lahko opazimo v celicah katerega koli tkiva. Značilno je, da mikronukleusi nastanejo kot posledica nenormalne celične delitve ali jedrne fragmentacije med apoptozo.
Homologna rekombinacija ali splošna rekombinacija je vrsta genetske rekombinacije, med katero se nukleotidna zaporedja izmenjajo med dvema podobnima ali identičnima kromosomoma. To je metoda, ki jo celice najpogosteje uporabljajo za popravilo poškodb dvoverižne ali enoverižne DNK. Homologna rekombinacija ustvarja tudi različne kombinacije genov med mejozo, kar zagotavlja visoko stopnjo dedne variabilnosti, kar omogoča populaciji, da se bolje prilagodi ...
Kozmidi (Cosmides) - plazmidi, ki vsebujejo fragment DNA lambda faga, vključno s cos-mesto. Skupaj s sistemi pakiranja fagnih delcev in vitro se uporabljajo kot vektorske molekule za kloniranje genov in pri gradnji genomskih knjižnic. Kozmide sta leta 1978 prva konstruirala Collins in Brüning. Njihovo ime izhaja iz okrajšave dveh izrazov: cos-section (izraz sam izhaja iz angleških kohezivnih koncev - lepljivih koncev) in plazmida.
Zaradi kopičenja ogromne količine informacij o genskih sekvencah se trenutno pogosto uporabljajo metode reverzne genetike za identifikacijo funkcij genov. Raziskovalci manipulirajo z zaporedji genov, spreminjajo ali izklapljajo določen gen in analizirajo, do kakšnih sprememb to vodi. To je pot obratne genetike: od gena do lastnosti/fenotipa. Genetika naprej in nazaj nista medsebojno izključujoča pristopa, ampak se dopolnjujeta pri preučevanju delovanja genov.
(eng. transformacija) - proces absorpcije molekule DNK iz zunanjega okolja s strani bakterijske celice. Da je celica sposobna transformacije, mora biti kompetentna, to pomeni, da morajo biti molekule DNK sposobne prodreti vanjo skozi celične membrane. Transformacija se aktivno uporablja v molekularni biologiji in genskem inženirstvu.
Nehomologno spajanje koncev ali nehomologno spajanje koncev (NHEJ) je eden od načinov popravljanja dvoverižnih prelomov v DNK. Ta proces imenujemo nehomoložni, ker so poškodovani konci verige povezani z ligazo neposredno, brez potrebe po homologni predlogi, v nasprotju s procesom homologne rekombinacije. Izraz "nehomologno spajanje koncev" sta leta 1996 predlagala Moore in Haber. NHEJ je bistveno manj natančen kot homologna rekombinacija ...
Cullins so družina hidrofobnih proteinov, ki služijo kot ogrodje za ubikvitinske ligaze (E3). Zdi se, da imajo vsi evkarionti kuline. Ti v kombinaciji z RING proteini tvorijo kulin-RING ubikvitinske ligaze (CRL), ki so zelo raznolike in igrajo vlogo pri številnih celičnih procesih, na primer pri proteolizi (uničijo približno 20 % celičnih proteinov), epigenetskem uravnavanju in imunost rastlin, posredovana s salicilno kislino.
Sekvenciranje naslednje generacije (NGS) je tehnika za določanje nukleotidnega zaporedja DNK in RNK, da dobimo formalni opis njene primarne strukture. Tehnologija metod sekvenciranja naslednje generacije (NGS) omogoča "branje" več delov genoma hkrati, kar je glavna razlika od prejšnjih metod sekvenciranja. SNP se izvaja s ponavljajočimi se cikli raztezanja verige, ki ga povzroči polimeraza, ali večkratnih...
Kvantiferon (včasih kvantiferon, quantiferon test; angleško QuantiFERON) je trgovsko ime za encimski imunski diagnostični test za okužbo s tuberkulozo, ki ga proizvaja ameriško podjetje QIAGEN. Besedilo uporablja tehnologijo ELISA za odkrivanje imunskega odziva na interferon gama.
Standardni mikroskopi ne omogočajo pregleda celic na molekularni ravni. Močno povečanje samo tukaj ni dovolj. Potrebni so digitalni posnetki, dodatni reagenti in drugi materiali ter instrumenti. Za analizo DNA in RNA se trenutno uporablja metoda, ki se imenuje in situ hibridizacija. Ker vključuje barvanje vzorcev, ki mu sledi analiza sevanja, se imenuje tudi fluorescenčna hibridizacija ali FISH.
Fluorescentna in situ hibridizacija se pogosto uporablja v genetskih raziskavah, diagnostiki raka, vodenju nosečnosti in na številnih drugih področjih znanosti. Metoda, kot že ime pove, temelji na lastnosti molekul DNK in RNK, da tvorijo stabilne vezi s sondami, torej tvorijo hibridne molekule. Besede "In situ" pomenijo, da so vsa opazovanja opravljena "in situ", torej neposredno brez uporabe dodatnega medija.
DNA sonde (sonde) so komplementarne molekulam v testnem vzorcu. Med njimi so nukleozidi, ki so označeni s fluorofori (snovi, ki dajejo molekuli lastnost fluorescence). Ta metoda se imenuje neposredno označevanje; če kot markerje uporabimo hibridne konjugirane molekule, dobimo posredno označevanje. Z neposrednim označevanjem lahko hibridizacijo opazujemo pod fluorescenčnim mikroskopom takoj po njenem zaključku. Za posredno označevanje se izvede še en postopek obarvanja. Po barvi loči konjugirane molekule od proučevanih vzorcev.
Metoda hibridizacije s posrednim označevanjem zahteva več časa in reagentov, vendar vam omogoča doseganje zanesljivejših rezultatov. Nivo signala bo v tem primeru višji, poleg tega pa je možno tudi njegovo postopno ojačanje. Klonirane sekvence DNA (produkti PCR, genomska DNA, označeni oligonukleotidi in drugi) se uporabljajo kot sonde za označevanje. Označevanje s sondo se izvaja na več načinov. Običajni metodi sta nick translacija in verižna reakcija s polimerazo (PCR) z označenimi nukleotidi.
Vrstni red postopka
In situ metoda se začne s pripravljalno fazo – načrtovanjem sond. Dimenzije sond ne smejo biti dovolj velike, da bi motile raziskovalni proces. Nezaželene so tudi premajhne sonde, saj ne zagotavljajo zanesljivih rezultatov. Zato se za raziskave vzamejo sonde velikosti do 1 tisoč bp. Če je sonda dvoverižna DNK, se kislina pred hibridizacijo denaturira. Ko je dosežen želeni rezultat (obarvani so določeni predeli kromosomov ali vsi kromosomi), je nadaljnja hibridizacija DNK sond s ponavljajočimi se sekvencami blokirana. Da bi to naredili, hibridizacijski mešanici dodamo neoznačene ponavljajoče se molekule DNK.
Naslednja stopnja raziskovanja je priprava preparatov interfaznih jeder oziroma metafaznih kromosomov. Celice se fiksirajo v substrat na steklu, nakar se DNK denaturira. Za znižanje temperature denaturacije in ohranitev morfologije jeder in kromosomov se denaturacija izvaja z dodatkom formadida. Nato materialu dodamo sonde in nekaj ur izvajamo hibridizacijo. Po njegovem zaključku se izvede večstopenjsko pranje, da se odstranijo sonde, ki se niso povezale z molekulami vzorca.
Vodja
"Onkogenetika"
Zhusina
Julia Gennadievna
Diplomiral na pediatrični fakulteti Voroneške državne medicinske univerze. N.N. Burdenko leta 2014.
2015 - pripravništvo v terapiji na podlagi Oddelka za fakultetno terapijo Voroneške državne medicinske univerze. N.N. Burdenko.
2015 - certifikacijski tečaj na specialnosti "Hematologija" na podlagi Hematološkega raziskovalnega centra v Moskvi.
2015-2016 – terapevt VGKBSMP št. 1.
2016 - odobrena je bila tema disertacije za diplomo kandidata medicinskih znanosti "študija kliničnega poteka bolezni in prognoze pri bolnikih s kronično obstruktivno pljučno boleznijo z anemičnim sindromom". Soavtor več kot 10 publikacij. Udeleženec znanstvenih in praktičnih konferenc o genetiki in onkologiji.
2017 - izpopolnjevanje na temo: "interpretacija rezultatov genetskih študij pri bolnikih z dednimi boleznimi."
Od leta 2017 rezidenca na specialnosti "Genetika" na podlagi RMANPO.
Vodja
"Genetika"
Kanivec
Ilja Vjačeslavovič

Kanivets Ilya Vyacheslavovich, genetik, kandidat medicinskih znanosti, vodja oddelka za genetiko medicinskega genetskega centra Genomed. Asistent Oddelka za medicinsko genetiko Ruske medicinske akademije za stalno strokovno izobraževanje.
Leta 2009 je diplomiral na Medicinski fakulteti Moskovske državne univerze za medicino in zobozdravstvo, leta 2011 pa je opravil specializacijo iz genetike na oddelku za medicinsko genetiko iste univerze. Leta 2017 je zagovarjal disertacijo za doktorat medicinskih znanosti na temo: Molekularna diagnostika variacij števila kopij segmentov DNA (CNV) pri otrocih s prirojenimi malformacijami, fenotipskimi anomalijami in/ali duševno zaostalostjo z uporabo oligonukleotidnih mikromrež visoke gostote SNP. »
Od leta 2011 do 2017 je delal kot genetik na Klinični kliniki za otroke. N.F. Filatov, znanstveno-svetovalni oddelek Zvezne državne proračunske znanstvene ustanove "Center za medicinske genetske raziskave". Od leta 2014 do danes je vodil genetski oddelek MHC Genomed.
Glavne dejavnosti: diagnostika in zdravljenje bolnikov z dednimi boleznimi in prirojenimi malformacijami, epilepsijo, medicinsko genetsko svetovanje družinam, v katerih je bil rojen otrok s dedno patologijo ali malformacijami, prenatalna diagnostika. Med svetovanjem se opravi analiza kliničnih podatkov in genealogije, da se določi klinična hipoteza in potrebna količina genetskega testiranja. Na podlagi rezultatov ankete se podatki interpretirajo in prejete informacije pojasnijo svetovalcem.
Je eden od ustanoviteljev projekta Šola genetike. Redno predstavlja predstavitve na konferencah. Predava za genetike, nevrologe in porodničarje-ginekologe ter za starše bolnikov z dednimi boleznimi. Je avtor in soavtor več kot 20 člankov in recenzij v ruskih in tujih revijah.
Področje strokovnega zanimanja je uvajanje sodobnih genomskih študij v klinično prakso, interpretacija njihovih rezultatov.
Sprejemni čas: sre, pet 16.-19
Vodja
"nevrologija"
Šarkov
Artem Aleksejevič

Šarkov Artjom Aleksejevič– nevrolog, epileptolog
Leta 2012 je študiral v okviru mednarodnega programa »Oriental medicine« na univerzi Daegu Haanu v Južni Koreji.
Od 2012 - sodelovanje pri organizaciji baze in algoritma za interpretacijo genetskih testov xGenCloud (https://www.xgencloud.com/, vodja projekta - Igor Ugarov)
Leta 2013 je diplomiral na Pediatrični fakulteti Ruske nacionalne raziskovalne medicinske univerze po imenu N.I. Pirogov.
Od leta 2013 do 2015 je študiral klinično specializacijo iz nevrologije na Zvezni državni proračunski znanstveni ustanovi "Znanstveni center za nevrologijo".
Od leta 2015 dela kot nevrolog, raziskovalec na Znanstvenoraziskovalnem kliničnem inštitutu za pediatrijo po imenu akademika Yu.E. Veltishchev GBOU VPO RNIMU im. N.I. Pirogov. Deluje tudi kot nevrolog in zdravnik v laboratoriju za video-EEG spremljanje v klinikah Centra za epileptologijo in nevrologijo po imenu A.I. A. A. Ghazaryan" in "Center za epilepsijo".
Leta 2015 se je izobraževal v Italiji na šoli »2nd International Residential Course on Drug Resistant Epilepsies, ILAE, 2015«.
Leta 2015 izpopolnjevanje - "Klinična in molekularna genetika za zdravnike", RCCH, RUSNANO.
V letu 2016 izpopolnjevanje - "Osnove molekularne genetike" pod vodstvom bioinformatike, dr. Konovalova F.A.
Od leta 2016 - vodja nevrološke smeri laboratorija "Genomed".
Leta 2016 se je izpopolnjeval v Italiji na šoli »San Servolo international advanced course: Brain Exploration and Epilepsy Surger, ILAE, 2016«.
Leta 2016 izpopolnjevanje - "Inovativne genetske tehnologije za zdravnike", "Inštitut za laboratorijsko medicino".
Leta 2017 - šola "NGS v medicinski genetiki 2017", Moskovski državni znanstveni center
Trenutno opravlja znanstvene raziskave na področju genetike epilepsije pod vodstvom prof.dr.med. Belousova E.D. in profesorica, d.m.s. Dadali E.L.
Odobrena je bila tema disertacije za diplomo kandidata medicinskih znanosti "Klinične in genetske značilnosti monogenih variant zgodnjih epileptičnih encefalopatij".
Glavna področja delovanja so diagnostika in zdravljenje epilepsije pri otrocih in odraslih. Ozka specializacija - kirurško zdravljenje epilepsije, genetika epilepsije. Nevrogenetika.
Znanstvene publikacije
Šarkov A., Šarkova I., Golovteev A., Ugarov I. "Optimizacija diferencialne diagnostike in interpretacija rezultatov genetskega testiranja s ekspertnim sistemom XGenCloud pri nekaterih oblikah epilepsije". Medicinska genetika, št. 4, 2015, str. 41.
*
Šarkov A.A., Vorobjov A.N., Troicki A.A., Savkina I.S., Dorofeeva M.Yu., Melikyan A.G., Golovteev A.L. "Kirurgija epilepsije pri multifokalnih možganskih lezijah pri otrocih s tuberozno sklerozo." Povzetki XIV ruskega kongresa "INOVATIVNE TEHNOLOGIJE V PEDIATRIJI IN OTROŠKI KIRURGiji". Ruski bilten perinatologije in pediatrije, 4, 2015. - str.226-227.
*
Dadali E.L., Belousova E.D., Šarkov A.A. "Molekularno genetski pristopi k diagnostiki monogene idiopatske in simptomatske epilepsije". Povzetek XIV ruskega kongresa "INOVATIVNE TEHNOLOGIJE V PEDIATRIJI IN OTROŠKI KIRURGiji". Ruski bilten perinatologije in pediatrije, 4, 2015. - str.221.
*
Šarkov A.A., Dadali E.L., Šarkova I.V. "Redka različica zgodnje epileptične encefalopatije tipa 2, ki jo povzročajo mutacije v genu CDKL5 pri moškem bolniku." Konferenca "Epileptologija v sistemu nevroznanosti". Zbirka konferenčnih gradiv: / Uredila: prof. Neznanova N.G., prof. Mikhailova V.A. Sankt Peterburg: 2015. - str. 210-212.
*
Dadali E.L., Šarkov A.A., Kanivets I.V., Gundorova P., Fominykh V.V., Šarkova I.V. Troitsky A.A., Golovteev A.L., Polyakov A.V. Nova alelna varianta mioklonusne epilepsije tipa 3, ki jo povzročajo mutacije v genu KCTD7 // Medicinska genetika.-2015.- v.14.-№9.- str.44-47
*
Dadali E.L., Šarkova I.V., Šarkov A.A., Akimova I.A. "Klinične in genetske značilnosti ter sodobne metode diagnostike dedne epilepsije". Zbirka gradiva "Molekularne biološke tehnologije v medicinski praksi" / Ed. dopisni član RANEN A.B. Maslennikova.- Št. 24.- Novosibirsk: Academizdat, 2016.- 262: str. 52-63
*
Belousova E.D., Dorofeeva M.Yu., Sharkov A.A. Epilepsija pri tuberozni sklerozi. V "Brain Diseases, Medical and Social Aspects", ki sta ga uredila Gusev E.I., Gekht A.B., Moskva; 2016; str.391-399
*
Dadali E.L., Šarkov A.A., Šarkova I.V., Kanivets I.V., Konovalov F.A., Akimova I.A. Dedne bolezni in sindromi, ki jih spremljajo febrilni krči: klinične in genetske značilnosti ter diagnostične metode. //Ruski časopis za otroško nevrologijo.- T. 11.- št. 2, str. 33-41. doi: 10.17650/ 2073-8803-2016-11-2-33-41
*
Šarkov A.A., Konovalov F.A., Šarkova I.V., Belousova E.D., Dadali E.L. Molekularno genetski pristopi k diagnostiki epileptičnih encefalopatij. Zbirka povzetkov "VI BALTIČKI KONGRES O OTROŠKI NEVROLOGIJI" / Uredila profesorica Guzeva V.I. Sankt Peterburg, 2016, str. 391
*
Hemisferotomija pri epilepsiji, odporni na zdravila, pri otrocih z obojestransko poškodbo možganov Zubkova N.S., Altunina G.E., Zemlyansky M.Yu., Troitsky A.A., Sharkov A.A., Golovteev A.L. Zbirka povzetkov "VI BALTIČKI KONGRES O OTROŠKI NEVROLOGIJI" / Uredila profesorica Guzeva V.I. Sankt Peterburg, 2016, str. 157.
*
*
Članek: Genetika in diferencirano zdravljenje zgodnjih epileptičnih encefalopatij. A.A. Šarkov*, I.V. Šarkova, E.D. Belousova, E.L. Dadali. Revija za nevrologijo in psihiatrijo, 9, 2016; Težava. 2doi:10.17116/jnevro20161169267-73
*
Golovteev A.L., Šarkov A.A., Troitsky A.A., Altunina G.E., Zemlyansky M.Yu., Kopachev D.N., Dorofeeva M.Yu. "Kirurško zdravljenje epilepsije pri tuberozni sklerozi" uredila Dorofeeva M.Yu., Moskva; 2017; str.274
*
Nove mednarodne klasifikacije epilepsije in epileptičnih napadov Mednarodne lige proti epilepsiji. Revija za nevrologijo in psihiatrijo. C.C. Korsakov. 2017. V. 117. št. 7. S. 99-106
Vodja
"Prenatalna diagnoza"
Kijev
Julija Kirillovna

Leta 2011 je diplomirala na Moskovski državni medicinski in stomatološki univerzi. A.I. Evdokimova z diplomo iz splošne medicine Študirala je na oddelku za medicinsko genetiko iste univerze z diplomo iz genetike
Leta 2015 je opravila pripravništvo iz porodništva in ginekologije na Medicinskem inštitutu za podiplomsko medicinsko izobraževanje Zvezne državne proračunske izobraževalne ustanove višjega strokovnega izobraževanja "MGUPP"
Od leta 2013 vodi posvetovalni termin v Centru za načrtovanje družine in reprodukcijo DZM.
Od leta 2017 je vodja oddelka za prenatalno diagnostiko laboratorija Genomed.
Redno predstavlja predstavitve na konferencah in seminarjih. Predava zdravnikom različnih specialnosti s področja reprodukcije in prenatalne diagnostike
Izvaja medicinsko genetsko svetovanje nosečnicam o prenatalni diagnostiki, da bi preprečili rojstvo otrok s prirojenimi malformacijami, pa tudi družine z domnevno dednimi ali prirojenimi patologijami. Izvaja interpretacijo dobljenih rezultatov DNK diagnostike.
SPECIALISTI
Latypov
Artur Šamilevič

Latypov Artur Shamilevich - zdravnik genetik najvišje kvalifikacijske kategorije.
Po diplomi na medicinski fakulteti Kazanskega državnega medicinskega inštituta leta 1976 je dolga leta delal najprej kot zdravnik v uradu za medicinsko genetiko, nato kot vodja medicinsko genetskega centra republiške bolnišnice Tatarstan, glavni specialist Ministrstvo za zdravje Republike Tatarstan, učitelj na oddelkih Kazanske medicinske univerze.
Avtor več kot 20 znanstvenih člankov o problemih reproduktivne in biokemijske genetike, udeleženec številnih domačih in mednarodnih kongresov in konferenc o problemih medicinske genetike. V praktično delo centra je uvedel metode množičnega presejanja nosečnic in novorojenčkov za dedne bolezni, opravil na tisoče invazivnih posegov pri sumu na dedne bolezni ploda v različnih obdobjih nosečnosti.
Od leta 2012 dela na Oddelku za medicinsko genetiko s predmetom prenatalne diagnostike na Ruski akademiji za podiplomsko izobraževanje.
Raziskovalno področje – presnovne bolezni pri otrocih, prenatalna diagnostika.
Čas sprejema: sre 12-15, sob 10-14Zdravniki se sprejemajo po dogovoru.
genetik
Gabelko
Denis Igorevič

Leta 2009 je diplomiral na medicinski fakulteti KSMU po imenu. S. V. Kurashova (specialnost "medicina").
Pripravništvo na Sankt Peterburški medicinski akademiji za podiplomsko izobraževanje Zvezne agencije za zdravje in socialni razvoj (specialnost "Genetika").
Pripravništvo v terapiji. Primarna prekvalifikacija v specialnosti "ultrazvočna diagnostika". Od leta 2016 je zaposlen na Oddelku Odseka za temelje klinične medicine Inštituta za fundamentalno medicino in biologijo.
Področje strokovnega zanimanja: prenatalna diagnostika, uporaba sodobnih presejalnih in diagnostičnih metod za prepoznavanje genetske patologije ploda. Ugotavljanje tveganja ponovitve dednih bolezni v družini.
Udeleženec znanstvenih in praktičnih konferenc o genetiki ter porodništvu in ginekologiji.
Delovne izkušnje 5 let.
Posvetovanje po dogovoruZdravniki se sprejemajo po dogovoru.
genetik
Grishina
Kristina Aleksandrovna

Leta 2015 je diplomirala na Moskovski državni medicinski in stomatološki univerzi iz splošne medicine. Istega leta je vstopila na specializacijo 30.08.30 "Genetika" v Zvezni državni proračunski znanstveni ustanovi "Center za medicinske genetske raziskave".
V Laboratoriju za molekularno genetiko kompleksno dednih bolezni (vodja - doktor bioloških znanosti Karpukhin A.V.) se je zaposlila marca 2015 kot raziskovalna laborantka. Od septembra 2015 je premeščena na delovno mesto raziskovalke. Je avtor in soavtor več kot 10 člankov in povzetkov o klinični genetiki, onkogenetiki in molekularni onkologiji v ruskih in tujih revijah. Redni udeleženec konferenc o medicinski genetiki.
Področje znanstvenih in praktičnih interesov: medicinsko genetsko svetovanje bolnikov z dedno sindromsko in multifaktorsko patologijo.
Posvetovanje z genetikom vam omogoča, da odgovorite na naslednja vprašanja:
Ali so simptomi pri otroku znaki dedne bolezni?
katere raziskave so potrebne za ugotovitev vzroka
določitev natančne napovedi
priporočila za izvajanje in vrednotenje rezultatov prenatalne diagnoze
vse, kar morate vedeti o načrtovanju družine
Posvetovanje o načrtovanju IVF
terenska in spletna svetovanja
udeležili znanstveno-praktične šole »Inovativne genetske tehnologije za zdravnike: uporaba v klinični praksi«, konference Evropskega združenja za humano genetiko (ESHG) in drugih konferenc, posvečenih humani genetiki.
Izvaja medicinsko genetsko svetovanje družinam z domnevno dednimi ali prirojenimi patologijami, vključno z monogenskimi boleznimi in kromosomskimi nepravilnostmi, določa indikacije za laboratorijske genetske študije, interpretira rezultate diagnostike DNK. Svetuje nosečnicam o prenatalni diagnostiki z namenom preprečevanja rojstva otrok s prirojenimi malformacijami.
Genetik, porodničar-ginekolog, kandidat medicinskih znanosti
Kudrjavceva
Elena Vladimirovna

Genetik, porodničar-ginekolog, kandidat medicinskih znanosti.
Specialistka na področju reproduktivnega svetovanja in dedne patologije.
Leta 2005 je diplomiral na Uralski državni medicinski akademiji.
Specializacija iz porodništva in ginekologije
Pripravništvo na specialnosti "Genetika"
Strokovna prekvalifikacija v specialnosti "ultrazvočna diagnostika"
Dejavnosti:
- Neplodnost in spontani splav Vasilisa Jurijevna

Diplomirala je na Medicinski fakulteti Državne medicinske akademije v Nižnem Novgorodu (specialnost "medicina"). Diplomirala je na kliničnem stažu FBGNU "MGNTS" z diplomo iz "Genetike". Leta 2014 je opravila pripravništvo na kliniki za materinstvo in otroštvo (IRCCS materno infantile Burlo Garofolo, Trst, Italija).
Od leta 2016 dela kot zdravnica svetovalka v podjetju Genomed LLC.
Redno sodeluje na znanstvenih in praktičnih konferencah o genetiki.
Glavne dejavnosti: Svetovanje o klinični in laboratorijski diagnostiki genetskih bolezni ter interpretacija rezultatov. Vodenje bolnikov in njihovih družin s sumom na dedno patologijo. Svetovanje pri načrtovanju nosečnosti, pa tudi med nosečnostjo o prenatalni diagnostiki, da bi preprečili rojstvo otrok s prirojeno patologijo.