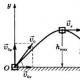
Eine Flüssigkeit, die niemals nass wird. Ergebnisse der Expertenbewertung. Adhäsions- und Kohäsionskräfte
Wenn Sie Sie fragen, woraus alles auf der Welt besteht – Wasser, Erde, Luft, Häuser, alle Dinge, Autos, Pflanzen und Tiere und schließlich wir selbst – was werden Sie antworten? Ich denke, Sie werden sagen: "Alles auf der Welt besteht aus winzigen, winzigen Teilchen - Atomen." Und Sie werden natürlich Recht haben ... aber nur teilweise. Jetzt werden Sie verstehen, was ich damit meine.
Stellen Sie sich vor, Sie stellen mir eine ähnliche Frage: „Woraus besteht der Text dieses Buches?“ Und ich werde antworten: „Aus Briefen!“ Und ich werde auch Recht haben, aber auch nur teilweise. Sie werden meine Antwort natürlich gleich ergänzen: „Der Text des Buches besteht aus Wörtern, und schon die Wörter bestehen aus Buchstaben!“
In der Tat, wenn Buchstaben nicht wüssten, wie man sie zu Wörtern zusammensetzt, wäre es unmöglich, selbst das einfachste Buch zu schreiben. Schließlich gibt es in unserem Alphabet nur dreiunddreißig Buchstaben - wie viele
sag es mir hier? Aber die Wörter, die aus diesen gleichen dreißig bestehen drei Buchstaben, - Tausende, und wie vielen sagen diese Worte verschiedene Geschichten wie viele Bücher, Lehrbücher, Lieder wurden geschrieben, Schulaufsätze, Notizen an die Eltern mit einer Einladung zur Schule, nur Briefe - es ist unmöglich zu zählen!
Es gibt mehr Atome „verschiedener Art“ als Buchstaben im Alphabet, aber immer noch nicht so viele: Jetzt, während ich diese Zeilen schreibe, gibt es einhundertsechs im „Atomalphabet“. verschiedene Atome, und nicht alle von ihnen kommen in der Natur vor - einige werden von Physikern künstlich gewonnen. Das bedeutet, wenn sich Atome nicht in verschiedenen Kombinationen miteinander verbinden könnten, gäbe es auf der Welt nur hundert verschiedene Substanzen. Es wäre eine furchtbar arme, langweilige und eintönige Welt – wie ein Buch, in dem auf der ersten Seite nur der Buchstabe „A“, auf der zweiten der Buchstabe „B“ stünde und so weiter …
Aber Sie wissen sehr wohl, dass die Welt so gar nicht ist! Sie könnten Tausende um sich herum zählen, ohne Ihr Zimmer zu verlassen verschiedene Substanzen. Insgesamt sind der Wissenschaft mittlerweile etwa zwei Millionen Substanzen mit unterschiedlichen Eigenschaften bekannt, und es werden täglich mehr. Eine solche Vielfalt ist nur möglich, weil sich Atome nicht schlechter als Buchstaben miteinander verbinden können.
WIE GLEICHE ATOM KOMBINIEREN...
Sag mir, wie viele Wörter hast du gesehen, die aus denselben Buchstaben bestehen? Eins-zwei – und verrechnet, oder? Und selbst dann bin ich mir nicht ganz sicher, ob man es wirkliche Worte nennen kann - eine Art Ausrufe und Onomatopöe: "Oh-oh"; "Uuuu..."; "rrr"; "Äh" ... Und alles in die gleiche Richtung.
Und was ist mit Atomen?
Nehmen Sie zum Beispiel ein Stück einer bekannten Substanz - Jod. Die braune Flüssigkeit, mit der Kratzer bestrichen werden, ist kein reines Jod, sondern Jodtinktur - eine Lösung von Jod in Alkohol. Aber in einer Apotheke können sie Ihnen reines Jod zeigen - Kristalle von einem schönen schwarzgrau mit lila Glitzer. In diesen Kristallen gibt es nur Jodatome, es gibt dort keine anderen Atome. Und doch, wenn sie dir einen solchen Kristall zeigen und fragen: „Was ist das kleinste Teilchen dieser Substanz?“ - beeilen Sie sich nicht zu antworten: "Natürlich das Jodatom, was sonst ?!" Denn Jodatome „sitzen“ in Kristallen zu zweit wie Schulkinder in einer Klasse. Aber die Jungs, die zusammen an einem Schreibtisch sitzen, zerstreuen sich nach der Schule in alle Richtungen, aber zwei zu einem Paar vereinte Jodatome trennen sich nicht, selbst wenn der Kristall schmilzt oder verdampft.
YODA
So „sitzen“ zweiatomige Jodmoleküle im Kristall.
Und wenn es uns dennoch gelänge, diese freundlichen Paare aufzubrechen – was wäre die Substanz einzelner Jodatome? Es scheint, welchen Unterschied macht es - schließlich sind die Atome gleich ... Aber es stellt sich heraus, dass es sich um eine Substanz mit völlig anderen Eigenschaften handelt. Und das bedeutet, dass ein Atom und zwei genau dieselben Atome, aber miteinander verbunden, nicht dasselbe sind!
Jetzt weißt du, wie du richtig antwortest, wenn sie dir einen Jodkristall zeigen und eine knifflige Frage stellen: „Was ist das kleinste Teilchen dieser Substanz?“ Sie werden antworten: "Zwei Jodatome gepaart!"
Übrigens gibt es ähnliche Fälle in der Welt der Wörter. Wenn wir kombinieren, sagen wir, zwei identische Wörter, "TAM", dann bekommt man ein neues Wort mit anderer Bedeutung - eine afrikanische Trommel. "TAMTAM".
Wenn Sie ein paar Tropfen Jodtinktur in ein Glasfläschchen gießen, stellen Sie das Fläschchen in Wasser und das Geschirr mit Wasser in Brand.
dann können Sie sehen, wie die Blase mit violetten Dämpfen gefüllt ist - sie bestehen aus zweiatomigen Jodmolekülen.
Das kleinste Teilchen einer Substanz, das noch die Eigenschaften dieser Substanz beibehält, wird MOLEKÜL genannt.
Wer also eine knifflige Frage nicht nur richtig, sondern auch wissenschaftlich beantworten will, nimmt einen Jodkristall und sagt: „Das kleinste Teilchen dieser Substanz ist ein Molekül, das aus zwei Jodatomen besteht.“
Sie und ich haben also festgestellt, dass ein Molekül einer Substanz vollständig aus zwei bestehen kann identische Atome. Und nicht nur das Jodmolekül – es gibt so viele solcher zweiatomigen Moleküle, wie Sie möchten! Sie sind wirklich von ihnen umgeben! Selbst jetzt, wenn Sie dieses Buch lesen, huschen Moleküle, die aus zwei identischen Atomen bestehen, um Sie herum und gelangen sogar in Ihre Lungen.
Natürlich haben Sie erkannt, dass wir über Luftmoleküle sprechen. Genauer gesagt um Stickstoffmoleküle und Sauerstoffmoleküle, aus denen die Luft hauptsächlich besteht.
Wenn sie sagen „Wir atmen Sauerstoff“, meinen sie Moleküle aus zwei Sauerstoffatomen. Und im Sauerstoffkissen, das schwerkranken Patienten gegeben wird, solche Moleküle, und in einer Stahlflasche mit komprimiertem Sauerstoff und in flüssigem Sauerstoff, der damit gefüllt ist Weltraumraketen, sind genau gleich
oder zweiatomige Moleküle. Aber warum betone ich so eindringlich, dass es sich genau um zweiatomige Moleküle handelt? Gibt es andere? Es gibt!
Während eines Gewitters werden Moleküle in der Luft gebildet, bestehend aus drei Atome Sauerstoff. Und dann sagen sie: "Der Geruch von Ozon." Das Gas, das aus dreiatomigen Sauerstoffmolekülen besteht, unterscheidet sich so sehr von dem Gas, das wir von zweiatomigen Molekülen gewohnt sind, dass sie ihm sogar einen anderen Namen gaben: Ozon.
Tatsächlich ist Sauerstoff geruchlos, aber Ozon riecht, und zwar ziemlich scharf („Ozon“ ist griechisch und bedeutet „riechend“).
Sauerstoff ist farblos und unsichtbar. Ozon ist sichtbar - es ist ein blaues Gas.
Wir atmen Sauerstoff, wir können kein Ozon atmen. Eine kleine Beimischung von Ozon verleiht der Luft zwar Frische, aber in in großen Zahlen Ozon ist ein schreckliches Gift!
Ozon ist eineinhalb Mal schwerer als Sauerstoff.
Flüssiger Sauerstoff ist hellblau, flüssiges Ozon ist dunkelviolett. Und diese Flüssigkeiten sieden bei unterschiedlichen Temperaturen.
Es ist kaum zu glauben, dass die Moleküle dieser beiden Substanzen aus genau denselben Atomen „zusammengesetzt“ sind. Allerdings, wie sie sagen, unglaublich, aber wahr!
WIE VERSCHIEDENE ATOM KOMBINIEREN
Aber wenn die Moleküle ein und derselben Atome so verschieden sind, welche Verschiedenheit muss es dann unter den Molekülen ein und derselben Atome geben? verschiedene Atome! Schauen wir noch einmal in die Luft – vielleicht finden wir dort solche Moleküle? Natürlich werden wir!
Wissen Sie, welche Moleküle Sie in die Luft ausatmen? (Natürlich nicht nur Sie - alle Menschen und alle Tiere.) Moleküle Ihres alten Freundes - Kohlendioxid! Kohlensäurebläschen prickeln angenehm auf der Zunge, wenn Sie Sprudelwasser oder Limonade trinken. Stücke Trockeneis
So „sitzen“ Kohlendioxidmoleküle in Trockeneiskristallen.
in Schachteln mit Eiscreme legen, bestehen ebenfalls aus solchen Molekülen; Trockeneis ist festes Kohlendioxid.
In einem Kohlendioxidmolekül haben sich zwei Sauerstoffatome miteinander verbunden verschiedene Parteien zu einem Kohlenstoffatom. "Carbon" bedeutet "derjenige, der Kohle gebiert". Aber aus Kohlenstoff entsteht mehr als nur Kohle. Wenn Sie mit einem einfachen Bleistift zeichnen, bleiben kleine Graphitflocken auf dem Papier – sie bestehen ebenfalls aus Kohlenstoffatomen. Diamant und gewöhnlicher Ruß werden aus ihnen „gemacht“. Wieder die gleichen Atome - und völlig unterschiedliche Substanzen!
Wenn sich Kohlenstoffatome nicht nur untereinander, sondern auch mit "fremden" Atomen verbinden, dann entstehen so viele verschiedene Substanzen, dass es schwierig ist, sie zu zählen! Besonders viele Stoffe entstehen, wenn sich Kohlenstoffatome mit Atomen des leichtesten Gases der Welt verbinden - Wasserstoff. Alle diese Substanzen werden genannt gemeinsamen Namen- Kohlenwasserstoffe, aber jeder Kohlenwasserstoff hat seinen eigenen Namen.
Der einfachste Kohlenwasserstoff wird in den Versen erwähnt, die Sie kennen: „Und in unserer Wohnung ist Gas einmal!“ Der Name des Gases, das in der Küche brennt, ist Methan. Das Methanmolekül hat ein Kohlenstoffatom und vier Wasserstoffatome. In der Flamme eines Küchenbrenners werden Methanmoleküle zerstört, ein Kohlenstoffatom verbindet sich mit zwei Sauerstoffatomen und es entsteht das bereits bekannte Kohlendioxidmolekül. Wasserstoffatome verbinden sich auch mit Sauerstoffatomen, und als Ergebnis werden Moleküle der wichtigsten und notwendigsten Substanz der Welt erhalten!
Moleküle dieser Substanz befinden sich auch in der Luft - dort gibt es viele davon. Daran sind Sie übrigens ein Stück weit beteiligt, denn Sie atmen diese Moleküle zusammen mit Kohlendioxidmolekülen in die Luft aus. Was ist diese Substanz? Wenn Sie es nicht erraten haben, atmen Sie auf das kalte Glas, und hier ist es vor Ihnen - Wasser!
Das Wassermolekül ist so winzig, dass, wenn wir hundert Millionen Wassermoleküle aneinanderreihen würden, diese ganze Linie locker zwischen zwei benachbarte Lineale in Ihrem Notizbuch passen würde. Trotzdem gelang es den Wissenschaftlern herauszufinden, wie ein Wassermolekül aussieht. Hier ist ihr Porträt. Es stimmt, es sieht aus wie der Kopf eines Bärenjungen Winnie the Pooh! Schau, wie du die Ohren gespitzt hast! Natürlich sind dies keine Ohren, sondern zwei Wasserstoffatome, die am „Kopf“ - dem Sauerstoffatom - befestigt sind. Aber Witze sind Witze, aber wirklich - haben diese "Ohren oben" etwas damit zu tun außergewöhnliche Eigenschaften Wasser!
WIE VERBINDEN UND LÖSEN MOLEKÜLE
Eine der bemerkenswertesten Eigenschaften von Wasser haben Sie im Winter an einem Fluss, an einem See oder an einem Teich schon hundertfach beobachtet. Hast du dort Eis gesehen? festes Wasser. Unter dem Eis flüssiges Wasser. Über dem Eis - Wasserdampf (es ist immer in der Luft). Was ist hier ungewöhnlich? Und hier ist was. Wasser ist die einzige Substanz auf der Erde, die das kann natürliche Bedingungen alle gleichzeitig drin sein drei Staaten: fest, flüssig und gasförmig!
Was sind diese drei Aggregatzustände? Wie unterscheiden sie sich und wie ähneln sie sich?
Betrachten wir zunächst die Substanz in fester Zustand. Sie wissen sehr gut, dass man, um etwas zu zerbrechen, Kraft aufwenden muss, manchmal beträchtliche. Die erste Schlussfolgerung kann gezogen werden: die Moleküle, aus denen sie bestehen fest sind fest miteinander verbunden. Sonst wäre alles, was wir solide nennen, längst zerfallen!
Sie wissen auch, dass eine feste Platte, bis sie geschmolzen oder zerbrochen wird, eine Platte in Form bleibt, ein Würfel ein Würfel bleibt, eine Röhre eine Röhre bleibt, eine Kugel eine Kugel bleibt ... Mit einem Wort, jeder feste Körper behält seine Form Form. Und wenn ja - Sie ziehen die zweite Schlussfolgerung - bedeutet dies, dass in Festkörper Es herrscht eine feste Ordnung: Jedes Molekül hat seine eigene bestimmter Ort, wie Soldaten in den Reihen (schließlich behält die Formation auch ihre Form, während die Soldaten auf ihren Plätzen bleiben).
Schließlich sind Sie sich dieser Eigenschaft wohl bewusst: Ein fester Körper lässt sich nur sehr schwer komprimieren. Was sagt es? Dass in einem Festkörper die Moleküle sehr dicht „gepackt“ sind – so dicht wie die Samen in einer Sonnenblume.
Dieselben Samen, aber in ein Glas gegossen, können mit flüssigen Molekülen verglichen werden - solche gibt es nicht mehr fester Auftrag, obwohl sie auch dicht „gepackt“ sind. Daher ist es schwierig, die Flüssigkeit zu komprimieren (Sie können dies sehen, wenn Sie Wasser in die Spritze ziehen, das Loch für die Nadel schließen und versuchen, den Kolben zu drücken! So werden auch die Moleküle in der Flüssigkeit dicht gepackt!
Sind flüssige Moleküle fest gebunden? Es scheint, dass
was für eine Kohäsion ist da, wenn sich ein Flüssigkeitsstrahl in Tropfen und ganz kleine Tröpfchen zerstreut ... Aber wissen Sie, wie viele Moleküle in einem winzigen Tröpfchen stecken? Es ist sogar beängstigend zu sagen: Milliarden von Milliarden! Es stellt sich heraus, dass in der Flüssigkeit die benachbarten Moleküle fest aneinander haften. Hälten sie nicht, würde der Strahl nicht in Tropfen zerfallen, sondern in einzelne Moleküle.
Sie und ich haben also festgestellt, dass sich eine Flüssigkeit und ein Feststoff in gewisser Weise ähneln: Die Moleküle in ihnen sind dicht gepackt, das heißt, sie befinden sich nahe beieinander, und gleichzeitig halten die benachbarten Moleküle „Hände “ fest.
Aber es gibt auch wichtiger Unterschied: dadurch, dass in einer flüssigkeit die moleküle keiner so strengen disziplin unterliegen wie in einem festen körper, behält die flüssigkeit nicht ihre form – einfach gesagt, sie fließt.
Vergleichen wir nun Flüssigkeit und Gas. Wenn Sie schon einmal einen Reifen mit einer Fahrradpumpe aufgepumpt haben, ist Ihnen wahrscheinlich aufgefallen, dass es im Gegensatz zu Flüssigkeit nichts kostet, Luft zu komprimieren. Ein Liter Luft kann, richtig gepresst, auf das Volumen eines Fingerhuts reduziert werden! Sie verstehen vollkommen, warum dies möglich ist: weil es große Lücken zwischen Luftmolekülen gibt. In der Tat, in Ihrem
In einem Raum beispielsweise ist der Abstand zwischen zwei benachbarten Luftmolekülen etwa zehnmal größer als die Größe des Moleküls selbst.
Vergleichen Sie Flüssigkeit und Gas in einer weiteren Eigenschaft. Sie haben also eine Tüte Milch gekauft, ihr Volumen beträgt einen halben Liter. In eine Flasche gegossen - der gleiche halbe Liter. In einem Glas, einem Topf, einer Kaffeekanne – Milch nimmt überall das gleiche Volumen ein.
Wie verhält sich das Gas? Es hat kein bestimmtes Volumen. Gasmoleküle zerstreuen sich bei der geringsten Gelegenheit in alle Richtungen, das heißt, wenn die Wände eines Gefäßes oder Raums sie nicht stören. Wenn Sie im Weltraum eine Gasdose öffnen, werden Gasmoleküle im ganzen Universum verteilt!
Davon werden Sie natürlich sofort profitieren wichtige Schlussfolgerung: nichts hält Gasmoleküle nahe beieinander. Es stellt sich heraus, dass jedes Gasmolekül dem berühmten ähnelt feenhafte katze, die "von selbst geht"!
Nun sehen Sie, was passiert: In einem Festkörper und in einer Flüssigkeit liegen benachbarte Moleküle nahe beieinander und sind fest miteinander verbunden. Gasmoleküle sind weit voneinander entfernt und es besteht kein Zusammenhalt zwischen ihnen. Sie ziehen also eine weitere wichtige Schlussfolgerung, dass die Kräfte, die Molekülen helfen, fest „Hände zu halten“ (Physiker nennen sie MOLEKULARE VERBINDUNGSKRÄFTE), nur auf sie wirken kurze Reichweite!
Aber kommen sich Gasmoleküle nie näher? Wie nah sie sind! Sie stoßen immer wieder aneinander: In Ihrem Zimmer beispielsweise zählt jedes Luftmolekül nicht weniger als vier Milliarden Kollisionen pro Sekunde!
Aber schließlich müssen sich die Luftmoleküle bei so vielen Kollisionen irgendwann an jeden einzelnen herantasten und sich „händchenhaltend“ zu Tröpfchen und Kristallen vereinen. Warum bilden sie sich nicht nach dem Vorbild von Wassermolekülen, Wolken und Nebeln, regnen nicht auf die Erde nieder, warum hat unser Planet nicht wenigstens kleine Bäche mit flüssigem Sauerstoff, Morgentau aus Flüssigstickstoff, Frost und Gletscher aus "Trockeneis" - festes Kohlendioxid? Was verhindert, dass sich die Moleküle dieser Gase bei der Annäherung verzahnen?
Beeinträchtigt die Geschwindigkeit. In demselben Raum rauschen Sauerstoff- und Stickstoffmoleküle mit einer Geschwindigkeit von etwa einem halben Kilometer pro Sekunde. Das sind 1800 Kilometer pro Stunde – das Eineinhalbfache schneller als Schall! (Denken Sie nur daran, dass dies Durchschnittsgeschwindigkeit: Es gibt Moleküle, die sowohl langsamer als auch schneller sind.)
Die Moleküle kollidieren mit hoher Geschwindigkeit und prallen wie Billardkugeln aneinander ab, ohne Zeit zu haben, sich zu verbinden.
Jetzt ist Ihnen klar, wie Sie den Gasmolekülen helfen können, zusammenzuhalten: Sie müssen ihre Geschwindigkeit verringern. Auf welche Weise? Kühlen Sie das Gas ab! Denn je höher die Temperatur, desto schneller bewegen sich die Moleküle. Umgekehrt, je niedriger die Temperatur, desto langsamer bewegen sich die Moleküle. Das bedeutet, dass jedes Gas so weit abgekühlt werden kann, dass es in eine Flüssigkeit und sogar in einen Feststoff übergeht!
Das muss man schon damals sagen thermische Bewegung Moleküle, obwohl es langsamer wird, aber nicht aufhört. Natürlich fliegen Moleküle in einem Feststoff und in einer Flüssigkeit nicht wie in einem Gas. In einem festen Körper „tanzen“ sie, ohne sich von ihrem Platz zu bewegen. Und in der Flüssigkeit wird das Molekül tanzen, an einer Stelle tanzen, dann - springen! - und tanzt nach einiger Zeit schon auf einem anderen - auf dem dritten und so weiter.
Die energiereichsten Moleküle können an die Oberfläche springen, sich von benachbarten Molekülen lösen und davonfliegen: Die Flüssigkeit verdunstet. Und wenn es zum Sieden erhitzt wird, lösen sich die Moleküle nicht nur an der Oberfläche, sondern auch im Inneren der Flüssigkeit, bis sich alles in Dampf verwandelt (man kann „in Gas“ sagen – das ist dasselbe).
Es ist ein Molekül Ameisensäure. Solche Moleküle werden von einer gestörten Ameise freigesetzt,
Wasserstoff- und Sauerstoffatome können sich nicht nur zu einem Wassermolekül, sondern auch zu einem solchen Wasserstoffperoxidmolekül verbinden.
WIE WASSERMOLEKÜLE ZUSAMMENKOMMEN
Aber hier ist das Erstaunliche: Sauerstoffmoleküle beginnen bei einer Temperatur von 183 Grad unter Null, Stickstoffmoleküle - sogar bei 196 Grad unter Null und Wasserdampfmoleküle - bei einer Temperatur von 100 Grad über Null zu Tröpfchen zu verschmelzen! Bei null Grad, wenn Sauerstoff und Stickstoff noch sehr weit entfernt von flüssig sind, verwandelt sich Wasser bereits in einen festen Körper – Eis!
Was ist los? Vielleicht fliegen Wasserdampfmoleküle langsamer als ihre Luftnachbarn - Sauerstoff-, Stickstoff- und Kohlendioxidmoleküle? Nur das Gegenteil! Wassermoleküle fliegen nicht langsamer, sondern schneller, weil sie fast doppelt so leicht sind wie Sauerstoffmoleküle und Stickstoffmoleküle, ganz zu schweigen von Kohlendioxidmolekülen. Was geschieht? Wenn Sauerstoff, Stickstoff u Kohlendioxid Gase bleiben unter natürlichen Bedingungen, Wasser auf der Erde und noch mehr sollte es ein Gas sein! Aber wir wissen beide, dass dem nicht so ist.
Das bedeutet, dass einige Kräfte dazu beitragen, dass sich Wassermoleküle trotz der enormen Geschwindigkeit bei Kollisionen zu Tröpfchen und Kristallen verbinden. Dank dieser Kräfte verhalten sich Wassermoleküle bei Kollisionen nicht wie Billardkugeln, sondern wie Klette: Sie berühren sich bei einem Treffen kaum - sie greifen sofort ineinander, und wenn sie ineinandergreifen, müssen Sie sie sehr gründlich schütteln, damit sie sich lösen. .
Was sind diese Kräfte?
Erinnern Sie sich, Sie und ich haben vorgeschlagen, dass zwei Wasserstoffatome, die Ohren in einem Wassermolekül ähneln, an seinen ungewöhnlichen Eigenschaften beteiligt sind? So ist es wirklich!
Auf diese beiden "Ohren", also auf Wasserstoffatome, könnte man das gleiche Zeichen setzen, das auf einer Seite der Batterie für eine Taschenlampe steht: "+" ("plus"). Und weiter gegenüberliegende Seite Wassermoleküle - ein Zeichen, das auf der anderen Seite der Batterie steht: "-" ("Minus"). Es stellt sich heraus, dass das Wassermolekül ein elektrisches Teilchen ist! Wie gut binden sie sich? elektrische Teilchen, können Sie selbst sehen: Führen Sie einen Plastikkamm durch trockenes Haar und bringen Sie es zu Papierfetzen. Wie kamen sie zusammen!
elektrische Kräfte, die Wassermolekülen bei der Bindung helfen, halten sie viel stärker zusammen als normale molekulare Kohäsionskräfte.
Ohne diese elektrischen Kräfte gäbe es kein Eis, keine Flüsse, keine Ozeane – schließlich wäre Wasser ein Gas!
Nein, schließlich haben wir großes Glück, dass Wassermoleküle so fest haften. Immerhin bestehen Sie und ich, wie alle Menschen, zu zwei Dritteln aus Wasser! Was soll ich sagen, denn wenn das Wasser nicht so wäre, würden wir nicht auf der Welt existieren, denn das Leben auf unserem Planeten hat seinen Ursprung im Wasser - im alten Ozean ...
WIE WASSERMOLEKÜLE MIT „ALIEN“-MOLEKÜLEN VERBINDEN
nicht. (In einem Glas und in jedem Glas an den Rändern, aber in einer Tube ist es auffälliger.) Was lässt es aufsteigen? Sie haben es wahrscheinlich selbst erraten: obwohl Wassermoleküle
Sie sind sehr stark miteinander verbunden, haften aber noch stärker an der Glasoberfläche.
Das heißt, das Glas ist NASS
Wasser.
Aber warum steigt dann das Wasser auf dem Glas nicht noch höher? Sie würde sich gerne erheben, aber das Gewicht lässt sie nicht: Die Adhäsionskräfte am Glas ziehen die Wassermoleküle nach oben und die Schwerkraft zieht sie nach unten.
Es gibt etliche Stoffe, die Wasser benetzt: Neben Glas sind das Porzellan, Metalle, viele Mineralien, vor allem Kreide und Gips …
Gibt es Stoffe, an denen Wassermoleküle schwächer haften als aneinander? So viel wie du willst! Schwefel, Graphit, Wachs, Paraffin, Naphthalin, Poly-
Nehmen Sie Wasser in die Pipette und sehen Sie es sich genau an: Sie sehen von oben keine ebene Fläche, sondern ein Loch - an den Rändern, am Glasröhrchen, ist das Wasser höher gestiegen als in der Mitte der Schüssel, das Wasser auch steigt an -
Äthylen, jedes Fett - all diese Substanzen werden NICHT durch Wasser nass. Der Milchbeutel besteht aus mit Paraffin imprägniertem Papier, und für solches Papier ist das Wasser überhaupt nicht nass: Halten Sie den Beutel unter den Wasserhahn und schütteln Sie ihn dann ab - es ist wie Wasser vom Rücken einer Ente! Übrigens ist Wasser für eine Gans nicht nass, weil ihre Federn gefettet sind.
Stellen Sie sich nun vor, Sie hätten die Aufgabe, einen Panzer mit zu bauen Wasser trinken für das Raumschiff. Welches Material würden Sie für den Tank wählen - das, bei dem das Wasser nass ist, oder das, bei dem "Wasser wie Wasser vom Rücken einer Ente ist"? Das heißt, was wird von Wasser benetzt oder was wird nicht benetzt?
BEI Raumschiff Es gibt keine Schwerkraft, also kann Wasser nicht fließen. Und die Kräfte des molekularen Zusammenhalts? Sie tun weiter wie bisher, als wäre nichts gewesen! Ich könnte das nicht sagen: Sie selbst verstehen vollkommen, dass, wenn die Kohäsionskräfte zwischen Molekülen nicht im Weltraum wirken würden, Raketen in den Weltraum geschossen würden und alles, was sich in ihnen befindet, in einzelne Moleküle zerfallen würde ...
Nehmen wir an, Sie haben einen Tank aus einem Material gebaut, an dem Wassermoleküle stärker haften als aneinander ... Nun, Glas zum Beispiel. Was wird passieren? Wasser beruhigt sich erst, wenn es die gesamte Oberfläche des Tanks von innen benetzt und mit einer gleichmäßigen Schicht bedeckt! Nicht nur das: Wenn Sie den Wasserhahn öffnen, tritt ein Teil des Wassers aus dem Tank, kriecht an seinen Wänden entlang und bedeckt den gesamten Tank und die Außenseite. Und es stellt sich heraus, dass kein Wasser im Tank ist, sondern ein Tank im Wasser!
Aber was passiert, wenn Sie einen Tank aus einem Material herstellen, das nicht von Wasser benetzt wird - beispielsweise aus Polyethylen? (Und der Kran natürlich auch...)
Jetzt kriecht das Wasser aus dem Tank nicht mehr von alleine! Und selbst wenn Sie den Wasserhahn ganz öffnen, fließt kein Tropfen heraus! Tatsächlich fließt auf der Erde Wasser aus einem Wasserhahn, wenn es unter dem Einfluss der Schwerkraft herunterfällt, aber hier wiegt Wasser nichts und fällt nirgendwo herunter.
Aber wie bekommt man Wasser aus dem Tank? Dort kann es beispielsweise mit einem Kolben herausgedrückt werden. Oder machen Sie die Wände des Tanks flexibel, elastisch und drücken Sie Wasser aus, als ob Zahnpasta aus einem Rohr. Anstelle eines Wasserhahns - ein flexibler Polyethylenschlauch mit Mundstück. Der Astronaut wollte trinken - er nahm das Mundstück mit den Lippen und das Wasser wird direkt in seinen Mund gepresst!
Wie Sie sehen, muss man schon bei der Entwicklung der „kleinen Dinge des Lebens“ für Astronauten wissen, in welchen Fällen das Wasser nass ist und in welchen nicht, und im Allgemeinen alle Gewohnheiten der Moleküle berücksichtigen .
Die schwarzen Kugeln repräsentieren hier, wie auch anderswo in diesem Buch, Kohlenstoffatome, blau – Wasserstoffatome, rot – Sauerstoffatome. gelber Ball ihr habt euch noch nicht getroffen. Es repräsentiert ein Atom des Leichtmetalls Natrium.
WIE MAN WASSER FÜR ALLE NASS MACHT
Warum ist Wasser bei manchen Stoffen nass und bei anderen nicht? Warum haften Wassermoleküle stärker an den Molekülen einiger Substanzen als aneinander und schwächer an den Molekülen anderer?
Als Wissenschaftler sich für den Unterschied zwischen Stoffen interessierten, die von Wasser benetzt werden, und Stoffen, die nicht benetzt werden, fanden sie dies heraus. Moleküle „wasserliebender“ Substanzen sind wie Wassermoleküle elektrische Teilchen! Darauf könnte man auch die Zeichen zeichnen, die auf Batterien für eine Taschenlampe stehen: „+“ und „-“ („Plus“ und „Minus“)! Deshalb haften Wassermoleküle so sehr an ihnen - wie man so schön sagt, ein Fischer sieht einen Fischer aus der Ferne!
Was ist mit gewöhnlichen, nichtelektrischen Molekülen? Es stellt sich heraus, dass auch sie der gleichen Regel folgen: Auch „ihre eigenen“, also gewöhnliche, nicht elektrische Moleküle haften gut an ihnen. Daher wird beispielsweise Ruß, der nicht von Wasser benetzt wird, perfekt von Fett benetzt ...
Nun, was wäre, wenn es notwendig wäre, eine Substanz mit Wasser ohne zu befeuchten? elektrische Moleküle? Kann das Wasser auch für sie nass gemacht werden?
Dürfen. Aber bevor ich erkläre, wie dies gemacht wird, werde ich beschreiben, wie in einigen südlichen Länder riesige Meeresschildkröten fangen.
Der Panzer einer Meeresschildkröte ist glatt und rutschig - nicht greifen, nicht festhalten. Und so Einheimische Sie ließen einen klebrigen Fisch am Schwanz an die Schildkröte binden. Dieser Fisch hat Saugnäpfe auf dem Rücken und klammert sich immer an jemanden: einen Hai, einen Wal, eine Schildkröte ... Ein klebriger Fisch bleibt sofort am Panzer haften und die Schildkröte wird zum Boot gezogen.
Es gibt also ein Molekül, das einem klebrigen Fisch ähnelt, der am Schwanz gebunden ist. Ein Ende ist elektrisch, das andere nicht. Ein Wassermolekül kann ein elektrisches Ende fest „packen“, und ein nichtelektrisches wird an einem Molekül haften bleiben, das für ein Wassermolekül schwer zu greifen ist – sagen wir, einem Fettmolekül – und es herausziehen. Wo? Ja, von überall - zum Beispiel von einem Teller. Oder von der Haut.
Nehmen wir an, Ihre Hände sind mit Fett verschmiert. Waschen Sie sie nur nicht mit Wasser. Und hier nehmen Sie die „klebrigen“ Moleküle … Nun, ich spreche natürlich von gewöhnlichen Seifenmolekülen!
Viele Leute denken, dass Seife und Wasser dank des Schaums reinigen - sie sagen, dass die Schaumblasen Schmutzpartikel einfangen und das Wasser sie wegspült. Jetzt sehen Sie, dass der Schaum nichts damit zu tun hat. Es gibt sogar Seifenarten, die überhaupt keinen Schaum bilden (z. B. Rizinusseife), aber nicht schlechter waschen als gewöhnliche!
So machen die Seifenmoleküle, wenn sie einmal im Wasser sind, es nass für jene Substanzen, die normalerweise vor Wasser „Angst“ haben. Wie wirken andere Moleküle auf Wasser?
Tropfen aus einer Pipette normales Wasser, und daneben - süß, und schauen Sie sich die Form der Tropfen an (denken Sie nur daran, dass die Oberfläche, auf die Sie tropfen, sauber sein muss).
Wenn die Oberfläche überhaupt nicht benetzt wird, bilden die Tropfen eine Kugel - genau wie Tau auf Blättern und Grashalmen. Ist die Oberfläche dagegen sehr gut benetzt, verteilen sich die Tropfen und bedecken sie mit einer dünnen Schicht. Nun, wenn es nicht sehr gut benetzt ist, aber nicht sehr schlecht, dann zeigt die Form der Tröpfchen sofort, für welche von ihnen das Wasser „feuchter“ ist!
Auf diese Weise können Sie untersuchen, wie nicht nur Zucker, sondern auch Salz die Benetzungseigenschaften von Wasser beeinflusst, Zitronensäure, Soda, Glycerin ... mit einem Wort, jede Substanz, die Sie bekommen können - solange sie sich in Wasser auflöst.
Hör zu, was ist, wenn du bei diesen Experimenten etwas entdeckst, das noch niemand beobachtet hat?!
Ich wünsche Ihnen Erfolg!
|||||||||||||||||||||||||||||||||
Buchtexterkennung aus Bildern (OCR) - Kreativstudio BK-MTGC.
pixabay.com
Warum Es regnet? Wo gehen Pfützen hin? Woher kommen die Babys? Warum habe ich Träume? Ein endloser Strom von Fragen fällt auf Eltern, die kleine Zappelbilder machen.
Die Herausgeberin eines amerikanischen Verlags, Gemma Harris, hatte die Idee, Kinder im Alter von 4 bis 12 Jahren zu bitten, ihr Fragen zu schicken, die sie ihren Müttern und Vätern stellen.
Ohne dumme und lustige zu bearbeiten oder wegzuwerfen, zeigte sie Fragen berühmte Schriftsteller, Wissenschaftler, Gastronomen, Reisende. Sie hat ihre Antworten in einem Buch mit dem Titel Why Is Water Wet? Und andere sehr wichtige Kinderfragen, die von sehr klugen Erwachsenen beantwortet werden." Behalte die Besten!
1. Warum entscheiden Erwachsene alles?
ottawafamilyliving.com
Antworten: Komikerin, Schauspielerin und Autorin Miranda Hart
„Um ehrlich zu sein, denke ich manchmal selbst darüber nach ... Mit zunehmendem Alter werden die Menschen in der Regel rekrutiert Lebenserfahrung, wodurch sie klüger werden und deshalb die meisten Entscheidungen treffen müssen.
Der Tag wird kommen, an dem Sie selbst erwachsen werden und alles, wovon ich spreche, vollständig verstehen können.“
2. Warum sind Kuchen so lecker?

„... Genau die gleiche Frage habe ich mir selbst schon oft gestellt. Einen Kuchen zu backen ist wie ein großer wissenschaftliches Experiment. Du gibst Eier, Butter, Zucker und Mehl in eine Schüssel, vermischst alles vorsichtig, schiebst es in den Ofen – und dann beginnt der Zauber! Und währenddessen ist es unglaublich schwierig, geduldig zu bleiben, denn der Ofen riecht wirklich köstlich.
Das Wichtigste ist, die Menge der einzelnen Produkte genau zu erraten, und dann wird der Kuchen so lecker, dass ich nicht anders kann, als ein breites Lächeln zu zeigen, wenn ich anfange, ihn zu essen. Diese Magie ist auch insofern bemerkenswert, als sie für jeden verfügbar ist.
3. Woher kommen Träume?

Antworten: Philosoph Alain de Botton
„Meistens sind Sie in der Lage, Ihren Geist zu kontrollieren. Willst du Lego spielen? Dein Gehirn wird dir dabei helfen. Beschlossen zu lesen? Bitte! Sie setzen Buchstaben in Worte und die Charaktere des Buches erwachen in Ihrer Vorstellung zum Leben.
Und nachts passiert etwas Seltsames. Während Sie im Bett schlafen, beginnt Ihr Bewusstsein, die unglaublichsten, erstaunlichsten und manchmal beängstigendsten Bilder zu zeigen ... Auf diese Weise wird unser Bewusstsein wieder aufgebaut und bringt sich nach dem nächsten Tag in Ordnung.
In deinen Träumen kehrst du zu dem zurück, was du tagsüber verpasst hast, erholst dich, träumst von angenehmen Dingen und erforschst die Ängste, die tagsüber tief, tief in deinem Geist verborgen sind.
4. Warum haben Menschen Musik erfunden?

Antworten: Rundfunksprecher und Musiker Jarvis Cocker
„Wenn wir morgen in einer Welt ohne Musik aufwachen würden, würde natürlich niemand sterben. Das ist schließlich weder Luft noch Wasser, es ist durchaus möglich, ohne Musik zu leben – aber stellen Sie sich vor, wie langweilig das Leben dann werden würde!
Einige Gelehrte glauben sogar, dass der Mensch zu singen und Musik zu komponieren begann, lange bevor er sprechen lernte. Es ist möglich, dass Musik die allererste Art der Kommunikation war. Schließlich hilft sie den Menschen immer noch, sich ohne Worte zu verstehen ... Deshalb sind die Menschen auf die Musik gekommen.
5. Warum langweile ich mich?

Antworten: Professor alte Geschichte, Autor des Buches Langeweile. lebende Geschichte» Peter Toohey
„Du langweilst dich, weil es nichts zu tun gibt. Freunde sind abgereist. Ich möchte draußen spielen gehen, aber ich muss ruhig und bewegungslos hinter verschlossenen Türen sitzen.
Langeweile ist die Aufforderung Ihres Körpers, Aktivitäten zu ändern, bevor Sie völlig traurig werden. In solchen Fällen wäre es gut, mit Familie oder Freunden irgendwohin zu gehen oder sich ein interessantes neues Geschäft zu suchen.
Kinder, Kinderfragen, Kindererziehung, Kindererziehung, Antworten auf Kinderfragen, Eltern, Eltern über Kindererziehung, wie man Kinderfragen beantwortet
Relevanz. Ich träume davon, Wissenschaftlerin zu werden und möchte lernen, Antworten auf meine Fragen zu finden.
Problem. Warum macht mich Wasser nass, und warum werde ich dann nicht nass wie ein Schwamm, sondern reibe mich nur mit einem Handtuch ab und bin wieder trocken.
Hypothese. Sie schlug vor, dass die Fähigkeit, andere Objekte zu benetzen, nicht nur vom Wasser abhängt, sondern auch von den Eigenschaften der Objekte, sodass einige Objekte mehr und andere weniger nass werden.
Der Zweck der Arbeit: die Hypothese zu beweisen oder zu widerlegen.
Aufgaben: Finden Sie die Zusammensetzung von Wasser heraus; bestimmen, wie nass sonstige Gegenstände; Identifizieren Sie, was die Fähigkeit von Wasser beeinflussen kann, andere Objekte zu benetzen oder zu benetzen. Studiengegenstand: Wasser. Studiengegenstand: Eigenschaft des Wassers.
Forschungsmethoden: Theorie, Experimente.
Ergebnisse. Aus der Enzyklopädie wurde herausgefunden, dass Wasser aus Molekülen besteht. Ein Molekül ist das kleinste Teilchen eines Stoffes. Elektrische Kräfte helfen Wassermolekülen, sich zu verbinden und fest zusammenzuhalten! Aber egal wie stark Wassermoleküle aneinander haften, sie können noch stärker an anderen Objekten haften. Halten Sie sich daran und machen Sie diese Gegenstände nass.
Versuche haben gezeigt:
- die Fähigkeit, nass zu werden oder nass zu werden, hängt nicht nur von den Eigenschaften des Wassers ab, sondern auch von den Eigenschaften anderer Gegenstände;
- Die Fähigkeit von Wassermolekülen, sich mit Objekten zu verbinden, kann sich ändern, wenn Wasser mit anderen Substanzen kombiniert wird.
Fazit: Die Hypothese wurde bestätigt. Die Fähigkeit, nass zu werden oder nass zu werden, hängt nicht nur von den Eigenschaften des Wassers ab, sondern auch von den Eigenschaften anderer Gegenstände.
Es wurde festgestellt, dass sich Wasser und Öl nicht miteinander vermischten und Tropfen mit Seife und Soda schnell verdunsteten. Diese Phänomene müssen untersucht werden.
Dateien:
- Text der Arbeit: Warum ist das Wasser nass? Stand 17.01.2018 13:19 (201,5 KB)
- Präsentation: Warum ist Wasser nass? Abgerufen am 17. Januar 2018, 13:19 Uhr (9,1 MB)
Ergebnisse der Expertenbewertung
Expertenkarte der Interbezirksphase 2017/2018 (Experten: 1)
Gesamtpunktzahl: 15
Kinder bringen Erwachsene oft in eine unangenehme Lage, indem sie nach einfachen, aber unverständlichen Dingen fragen. "Warum ist das Wasser nass?" - eine der unbequemsten Kinderfragen.
Wenn sie danach fragen, wollen die Kinder ihren Horizont erweitern, wissen die Umwelt Allerdings hat nicht jeder Elternteil genügend Schul- bzw Naturwissenschaften klar und richtig zu beantworten. Und doch, warum ist das Wasser nass? Versuchen wir es herauszufinden.
Was bedeutet das Wort „nass“?
Die meisten Wörterbücher und Enzyklopädien nennen einen Gegenstand „nass“ oder einen Gegenstand, der Feuchtigkeit ausgesetzt wurde, mit einer Flüssigkeit in Kontakt kommt. BEI wissenschaftliches Verständnis Das Wort "nass" bezieht sich auf die Fähigkeit einer Flüssigkeit, an der Oberfläche fester Materialien zu haften.
Diese Eigenschaften hat nicht nur Wasser. Beispielsweise gilt flüssiges Helium als das feuchteste. Bei Temperaturen unter -270 °C verliert es seine Viskosität und wird sehr dünnflüssig.
Aus dem Vorstehenden können wir schließen, dass nicht das Wasser selbst nass ist, sondern die Gegenstände, auf die es fällt. Allerdings kann nicht jeder mit Flüssigkeit bedeckte Gegenstand nass sein. 
Insbesondere Wasser aus mit großer Mühe benetzt Metalle und ist völlig unfähig, fettige Oberflächen und Paraffine zu benetzen. An polymeren Materialien wie Polyethylen oder Kunststoff perlen Wassertropfen leicht ab.
Woraus besteht Wasser?
Warum werden manche Gegenstände durch die Flüssigkeit nass, andere nicht? Es kommt auf die Zusammensetzung des Wassers an. Sie repräsentiert anorganische Verbindung besteht aus polaren Molekülen. Jedes enthält ein Sauerstoffatom und zwei Wasserstoffatome.
Beide Substanzen sind schwerer als Luft, aber die Sauerstoffatome in den Molekülen sind positiv geladen und die Wasserstoffatome sind negativ geladen. Diese Potentialdifferenz ermöglicht es der Flüssigkeit, eine schwache elektrische Verbindung mit anderen Objekten herzustellen.
Aufgrund der Polarität der Moleküle kann sich Wasser an festen Oberflächen anlagern und diese benetzen. Wenn Sie Regen ausgesetzt waren, wurde Ihre Kleidung mit Wasserpartikeln bedeckt und saugte sie auf und wurde nass. 
Wenn man sich die Hände unter dem Wasserhahn wäscht, dann haben sich auch Wassermoleküle auf sie gesetzt, sich mit der Haut verbunden und sie nass gemacht. Gleichzeitig kann die Flüssigkeit mit ihrer Fähigkeit, das Volumen beizubehalten, ihre Form überhaupt nicht halten, daher fließt sie, wenn sie auf Gegenstände trifft, an ihnen herunter.
Welche Eigenschaften hat Wasser?
Wasser ist eine einzigartige Substanz, die unterschiedliche Bedingungen kann in drei sein verschiedene Staaten Flüssigkeit, Dampf und Feststoff. BEI normale Bedingungen es bleibt flüssig, bei Temperaturen unter 0 °C gefriert es und wird zu Eis, und bei erhöhte Temperaturen verdunstet und wird zu Dampf. Eismoleküle sind inaktiv und eng miteinander verwandt, sodass sie feste Objekte nicht durchdringen können.
Wenn sich Wasser in einem flüssigen oder dampfförmigen Zustand befindet, wird eine schwache Beziehung zwischen den Molekülen beobachtet, aber sie sind beweglicher als in einem gefrorenen, wodurch sie sich unter mechanischer Einwirkung leicht voneinander trennen und an die Moleküle von binden andere Substanzen.
Die Fähigkeit, sich auf verschiedenen Oberflächen zu vermischen und zu halten, ermöglicht es ihnen, in die Poren fester Gegenstände einzudringen und sie nass zu machen. Wassermoleküle scheinen an diesen Objekten zu haften und wirken wie "Schleim".
Warum ist das Wasser nass?
Zusammenfassend lässt sich sagen, dass Wasser nass ist, vor allem weil es seinem Aggregatzustand nach flüssig ist. Zweitens erzeugt es aufgrund seiner geringen Formbeständigkeit, niedrigeren Viskosität und Polarität in der molekularen Zusammensetzung ein nasses Gefühl. 
Wenn ein Kind diese Frage beantworten muss, kann man einfach sagen, dass Wasser aus kleinen Tröpfchen besteht, die nicht gut aneinander haften und sich ständig ausbreiten. Und natürlich ist es erwähnenswert, dass nicht das Wasser tatsächlich nass ist, sondern die Gegenstände, die es benetzt hat.